Тепловой эффект химической реакции
| Загрузить архив: | |
| Файл: ref-21046.zip (38kb [zip], Скачиваний: 133) скачать |
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
Воронежский государственный технический университет
КУРСОВОЙ ПРОЕКТ
по дисциплине «Теоретические основы прогрессивной технологии»
Тема: «Тепловой эффект химической реакции и его практическое применение.»
|

Воронеж 2004
Содержание
|
Введение …………………………………………………………………… |
3 |
|
1. Тепловой эффект химической реакции………………………………... |
4 |
|
1.1. Уравнения химических реакций……………………………... |
8 |
|
1.2. Основные законы термохимии………………………………. |
10 |
|
2. Применение теплового эффекта на практике…………………………. |
12 |
|
2.1.Жаропрочные покрытия………………………………………. |
1 |
|
2.2.Термохимический способ обработки алмаза………………... |
14 |
|
2.3.Техногенное сырьё для производства цемента……………… |
15 |
|
2.4. Биосенсоры……………………………………………………. |
16 |
|
Заключение…………………………………………………………………. |
17 |
|
Список литературы………………………………………………………… |
18 |
Введение
Тепловые эффекты химических реакций необходимы для многих технических расчетов. Они находят обширное применение во многих отраслях промышленности, а также в военных разработках.
Целью данной курсовой работы является изучение практического применения теплового эффекта. Мы рассмотрим некоторые варианты его использования, и выясним насколько важноиспользование тепловых эффектов химических реакций в условиях развития современных технологий.
1. Тепловой эффект химической реакции
В каждом веществе запасено определенное количество энергии. С этим свойством веществ мы сталкиваемся уже за завтраком, обедом или ужином, так как продукты питания позволяют нашему организму использовать энергию самых разнообразных химических соединений, содержащихся в пище. В организме эта энергия преобразуется в движение, работу, идет на поддержание постоянной (и довольно высокой!) температуры тела.
Одним из самых известных ученых, работающих в области термохимии, является Бертло. Бертло- профессор химии Высшей фармацевтической школы в Париже (1859г). Министр просвещения и иностранных дел.
Начиная с 1865 Бертло активно занимался термохимией, провел обширные калориметрические исследования, приведшие, в частности, к изобретению "калориметрической бомбы" (1881); ему принадлежат понятия "экзотермической" и "эндотермической" реакций. Бертло получены обширные данные о тепловых эффектах огромного числа реакций, о теплоте разложения и образования многих веществ.
Бертло исследовал действие взрывчатых веществ: температуру взрыва, скорости сгорания и распространения взрывной волны и др.
Энергия химических соединений сосредоточена главным образом в химических связях. Чтобы разрушить связь между двумя атомами, требуется затратить энергию. Когда химическая связь образуется, энергия выделяется.
Любая химическая реакция заключается в разрыве одних химических связей и образовании других.
Когда в результате химической реакции при образовании новых связей выделяется энергии больше, чем потребовалось для разрушения "старых" связей в исходных веществах, то избыток энергии высвобождается в виде тепла. Примером могут служить реакции горения. Например, природный газ (метан CH4) сгорает в кислороде воздуха с выделением большого количества теплоты (рис. 1а). Такие реакции являются экзотермическими.
· Реакции, протекающие с выделением теплоты, проявляют положительный тепловой эффект (Q>0, DH<0) и называются экзотермическими.
В других случаях на разрушение связей в исходных веществах требуется энергии больше, чем может выделиться при образовании новых связей. Такие реакции происходят только при подводе энергии извне и называются эндотермическими.
· Реакции, которые идут с поглощением теплоты из окружающей среды (Q<0, DH>0), т.е. с отрицательным тепловым эффектом, являются эндотермическими.
Примером является образование оксида углерода (II) CO и водорода H2 из угля и воды, которое происходит только при нагревании (рис. 1б).
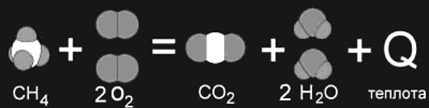
Рис. 1а
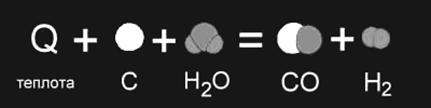
Рис. 1б
Рис. 1а,б. Изображение химических реакций при помощи моделей молекул: а) экзотермическая реакция, б) эндотермическая реакция. Модели наглядно показывают, как при неизменном числе атомов между ними разрушаются старые и возникают новые химические связи.
Таким образом, любая химическая реакция сопровождается выделением или поглощением энергии. Чаще всего энергия выделяется или поглощается в виде теплоты (реже - в виде световой или механической энергии). Эту теплоту можно измерить. Результат измерения выражают в килоджоулях (кДж) для одного моля реагента или (реже) для моля продукта реакции. Такая величина называется тепловым эффектом реакции.
- Тепловой эффект - количество теплоты, выделившееся или поглощенное химической системой при протекании в ней химической реакции.
Тепловой эффект обозначается символами Q или DH (Q = -DH). Его величина соответствует разности между энергиями исходного и конечного состояний реакции:
DH = Hкон.- Hисх. = Eкон.- Eисх.
Значки (г), (ж) обозначают газообразное и жидкое состояние веществ. Встречаются также обозначения (тв) или (к) - твердое, кристаллическое вещество, (водн) - растворенное в воде вещество и т.д.
Обозначение агрегатного состояния вещества имеет важное значение. Например, в реакции сгорания водорода первоначально образуется вода в виде пара (газообразное состояние), при конденсации которого может выделиться еще некоторое количество энергии. Следовательно, для образования воды в виде жидкости измеренный тепловой эффект реакции будет несколько больше, чем для образования только пара, поскольку при конденсации пара выделится еще порция теплоты.
Используется также частный случай теплового эффекта реакции - теплота сгорания. Из самого названия видно, что теплота сгорания служит для характеристики вещества, применяемого в качестве топлива. Теплоту сгорания относят к 1 молю вещества, являющегося топливом (восстановителем в реакции окисления), например:
|
C2H2 |
+ |
2,5 O2 |
= |
2 CO2 |
+ |
H2O |
+ |
1300 кДж |
|
ацетилен |
теплота сгорания ацетилена |
Запасенную в молекулах энергию (Е) можно отложить на энергетической шкале. В этом случае тепловой эффект реакции (D Е) можно показать графически (рис. 2).
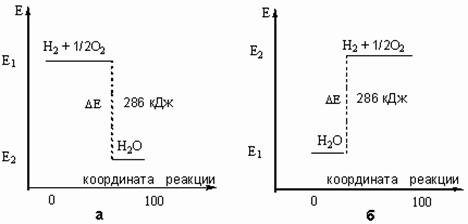
Рис. 2. Графическое изображение теплового эффекта (Q = D Е): а) экзотермической реакции горения водорода; б) эндотермической реакции разложения воды под действием электрического тока. Координату реакции (горизонтальную ось графика) можно рассматривать, например, как степень превращения веществ (100% - полное превращение исходных веществ).
1.1. Уравнения химических реакций
· Уравнения химических реакций, в которых вместе с реагентами и продуктами записан и тепловой эффект реакции, называются термохимическими уравнениями.
Особенность термохимических уравнений заключается в том, что при работе с ними можно переносить формулы веществ и величины тепловых эффектов из одной части уравнения в другую. С обычными уравнениями химических реакций так поступать, как правило, нельзя.
Допускается также почленное сложение и вычитание термохимических уравнений. Это бывает нужно для определения тепловых эффектов реакций, которые трудно или невозможно измерить в опыте.
Приведем пример. В лаборатории чрезвычайно трудно осуществить "в чистом виде" реакцию получения метана СH4 путем прямого соединения углерода с водородом:
С + 2 H2 = СH4
Но можно многое узнать об этой реакции с помощью вычислений. Например, выяснить, будет эта реакция экзо- или эндотермической, и даже количественно рассчитать величину теплового эффекта.
Известны тепловые эффекты реакций горения метана, углерода и водорода (эти реакции идут легко):
а) СH4(г) + 2 O2(г) = СO2(г) + 2 H2О(ж) + 890 кДж
б) С(тв) + O2(г) = СO2(г) + 394 кДж
в) 2 H2(г) + O2(г) = 2 H2О(ж) + 572 кДж
Вычтем два последних уравнения (б) и (в) из уравнения (а). Левые части уравнений будем вычитать из левой, правые - из правой. При этом сократятся все молекулы O2, СO2 и H2О. Получим:
СH4(г) - С(тв) - 2 H2(г) = (890 - 394 - 572) кДж = -76 кДж
Это уравнение выглядит несколько непривычно. Умножим обе части уравнения на (-1) и перенесем CH4 в правую часть с обратным знаком. Получим нужное нам уравнение образования метана из угля и водорода:
С(тв) + 2 H2(г) = CH4(г) + 76 кДж/моль
Итак, наши расчеты показали, что тепловой эффект образования метана из углерода и водорода составляет 76 кДж (на моль метана), причем этот процесс должен быть экзотермическим (энергия в этой реакции будет выделяться).
Важно обращать внимание на то, что почленно складывать, вычитать и сокращать в термохимических уравнениях можно только вещества, находящиеся в одинаковых агрегатных состояниях, иначе мы ошибемся в определении теплового эффекта на величину теплоты перехода из одного агрегатного состояния в другое.
1.2. Основные законы термохимии
· Раздел химии, занимающийся изучением превращения энергии в химических реакциях, называется термохимией.
Существует два важнейших закона термохимии. Первый из них, закон Лавуазье–Лапласа, формулируется следующим образом:
· Тепловой эффект прямой реакции всегда равен тепловому эффекту обратной реакции с противоположным знаком.
Это означает, что при образовании любого соединения выделяется (поглощается) столько же энергии, сколько поглощается (выделяется) при его распаде на исходные вещества. Например:
2 H2(г) + O2(г) 2 H2О(ж) + 572 кДж (горение водорода в кислороде)
2 H2О(ж) + 572 кДж = 2 H2(г) + O2(г) (разложение воды электрическим током)
Закон Лавуазье–Лапласа является следствием закона сохранения энергии.
Второй закон термохимии был сформулирован в 1840 г российским академиком Г. И. Гессом:
· Тепловой эффект реакции зависит только от начального и конечного состояния веществ и не зависит от промежуточных стадий процесса.
Это означает, что общий тепловой эффект ряда последовательных реакций будет таким же, как и у любого другого ряда реакций, если в начале и в конце этих рядов одни и те же исходные и конечные вещества. Эти два основных закона термохимии придают термохимическим уравнениям некоторое сходство с математическими, когда в уравнениях реакций можно переносить члены из одной части в другую, почленно складывать, вычитать и сокращать формулы химических соединений. При этом необходимо учитывать коэффициенты в уравнениях реакций и не забывать о том, что складываемые, вычитаемые или сокращаемые моли вещества должны находиться в одинаковом агрегатном состоянии.
2. Применение теплового эффекта на практике
Тепловые эффекты химических реакций нужны для многих технических расчетов. Например, рассмотрим мощную российскую ракету "Энергия", способную выводить на орбиту космические корабли и другие полезные грузы. Двигатели одной из её ступеней работают на сжиженных газах - водороде и кислороде.
Допустим, нам известна работа (в кДж), которую придется затратить для доставки ракеты с грузом с поверхности Земли до орбиты, известна также работа по преодолению сопротивления воздуха и другие затраты энергии во время полета. Как рассчитать необходимый запас водорода и кислорода, которые (в сжиженном состоянии) используются в этой ракете в качестве топлива и окислителя?
Без помощи теплового эффекта реакции образования воды из водорода и кислорода сделать это затруднительно. Ведь тепловой эффект - это и есть та самая энергия, которая должна вывести ракету на орбиту. В камерах сгорания ракеты эта теплота превращается в кинетическую энергию молекул раскаленного газа (пара), который вырывается из сопел и создает реактивную тягу.
В химической промышленности тепловые эффекты нужны для расчета количества теплоты для нагревания реакторов, в которых идут эндотермические реакции. В энергетике с помощью теплот сгорания топлива рассчитывают выработку тепловой энергии.
Врачи-диетологи используют тепловые эффекты окисления пищевых продуктов в организме для составления правильных рационов питания не только для больных, но и для здоровых людей - спортсменов, работников различных профессий. По традиции для расчетов здесь используют не джоули, а другие энергетические единицы - калории (1 кал = 4,1868 Дж). Энергетическое содержание пищи относят к какой-нибудь массе пищевых продуктов: к 1 г, к 100 г или даже к стандартной упаковке продукта. Например, на этикетке баночки со сгущенным молоком можно прочитать такую надпись: "калорийность 320 ккал/100 г".
Тепловой эффект рассчитывается при получении монометиланилина, который относится к классу замещенных ароматических аминов. Основная область применения монометиланилина – антидетонационная присадка для бензинов. Возможно использование монометиланилина в производстве красителей. Товарный монометиланилин (N-метиланилин) выделяется из катализата методом периодической или непрерывной ректификации. Тепловой эффект реакции ∆Н= -14±5 кДж/моль.
2.1.Жаропрочные покрытия
Развитие техники высоких температур вызывает необходимость создания особо жаропрочных материалов. Эта задача может быть решена путём использования тугоплавких и жаропрочных металлов. Интерметаллические покрытия привлекают всё большее внимание, поскольку обладают многими ценными качествами: стойкостью к окислению, агрессивными расплавами, жаропрочностью и т.д. Интерес представляет и существенная экзотермичность образования этих соединений из составляющих их элементов.Возможны два способа использования экзотермичности реакции образования интерметаллидов. Первый – получение композитных, двухслойных порошков. При нагреве компоненты порошка вступают во взаимодействие, и тепло экзотермической реакции компенсируют остывание частиц, достигающих защищаемой поверхности в полностью расплавленном состоянии и образующих малопористое прочно сцеплённое с основой покрытие. Другим вариантом может быть нанесение механической смеси порошков. При достаточном нагреве частиц они вступают во взаимодействие уже в слое покрытие. Если величина теплового эффекта значительная, то это может привести к самопроплавлению слоя покрытия, образованию промежуточного диффузионного слоя, повышающего прочность сцепления, получения плотной, малопористой структуры покрытия. Пpи выборе композиции, образующей интерметаллидное покрытие с большим тепловым эффектом и обладающее многими ценными качествами – коррозионной стойкостью, достаточной жаропрочностью и износостойкостью, обращает на себя внимание алюминиды никеля, в частности NiAl и Ni3Al. Образование NiAl сопровождается максимальным тепловым эффектом.
2.2.Термохимический способ обработки алмаза
Свое название "термохимический" способ получил благодаря тому, что протекает он при повышенных температурах, а в основе его лежит использование химических свойств алмаза. Осуществляется способ следующим образом: алмаз приводят в контакт с металлом, способным растворять в себе углерод, а для того, чтобы процесс растворения или обработки шел непрерывно, его проводят в атмосфере газа, взаимодействующего с растворенным в металле углеродом, но не реагирующим непосредственно с алмазом. В процессе величина теплового эффекта принимает высокое значение.
Для определения оптимальных условий проведения термохимической обработки алмаза и выявления возможностей способа потребовалось изучить механизмы определенных химических процессов, которые, как показал анализ литературы, вообще не исследовались. Более конкретному изучению термохимической обработки алмаза мешало, прежде всего, недостаточное знание свойств самого алмаза. Опасались испортить его нагревом. Исследования по термической устойчивости алмаза были выполнены лишь в последние десятилетия. Установлено, что алмазы, не содержащие включений, в нейтральной атмосфере или в вакууме можно без всякого для них вреда нагреть до 1850 “С”, и только выше.
Алмаз является лучшим материалом для лезвия благодаря уникальной твердости, упругости и низкому трению по биологическим тканям. Оперирование алмазными ножами облегчает проведение операций, сокращает в 2-3 раза сроки заживления разрезов. По мнению микрохирургов МНТК микрохирургии глаза, ножи, заточенные термохимическим способом, не только не уступают, но и превосходят по качеству лучшие зарубежные образцы. Термохимически заточенными ножами уже сделаны тысячи операций. Алмазные ножи разной конфигурации и размеров могут применяться и в других областях медицины, биологии. Так, для изготовления препаратов в электронной микроскопии используют микротомы. Высокая разрешающая способность электронного микроскопа предъявляет особые требования к толщине и качеству среза препаратов. Алмазные микротомы, заточенные термохимическим методом, позволяют изготавливать срезы нужного качества.
2.3. Техногенное сырьё для производства цемента
Дальнейшая интенсификация цементного производства предполагает широкое внедрение энерго- и ресурсосберегающих технологий с использованием отходов различных отраслей.
При переработке скарново-магнетитовых руд выделяются хвосты сухой магнитной сепарации (СМС), представляющие собой щебневидный материал с размером зерен до 25 мм. Хвосты СМС имеют достаточно стабильный химический состав, мас.%: SiO2 40…45, Al 2O3 10…12, Fe2O3 15…17, CaO 12…13, MgO 5…6, S 2…3, R2O 2…4. Доказана возможность использования хвостов СМС в производстве портландцементного клинкера. Полученные цементы характеризуются высокими прочностными показателями.
Тепловой эффект клинкерообразования (ТЭК) определен как алгебраическая сумма теплот эндотермических процессов (декарбонизация известняка, дегидратация минералов глины, образование жидкой фазы) и экзотермических реакций (окисление пирита, вносимого хвостами СМС, формирование клинкерных фаз).
Основными преимуществами использования отходов обогащения скарново-магнетитовых руд в производстве цемента являются:
- расширение сырьевой базы за счет техногенного источника;
- экономия природного сырья при сохранении качества цемента;
- снижение топливно-энергетических затрат на обжиг клинкера;
- возможность выпуска малоэнергоемких активных низкоосновных клинкеров;
- решение экологических проблем за счет рациональной утилизацииотходов и сокращения газовых выбросов в атмосферу при обжиге клинкера.
2.4. Биосенсоры
Биосенсоры - датчики на основе иммобилизованных ферментов. Позволяют быстро и качественно анализировать сложные, многокомпонентные смеси веществ. В настоящее время находят все более широкое применение в целом ряде отраслей науки, промышленности, сельского хозяйства и здравоохранения. Основой для создания автоматических систем ферментативного анализа послужили последние достижения в области энзимологии и инженерной энзимологии. Уникальные качества ферментов - специфичность действия и высокая каталитическая активность - способствуют простоте и высокой чувствительности этого аналитического метода, а большое количество известных и изученных на сегодняшний день ферментов позволяют постоянно расширять список анализируемых веществ.
Ферментные микрокалориметрические датчики - используют тепловой эффект ферментативной реакции. Состоит из двух колонок (измерительной и контрольной), заполненных носителем с иммобилизованным ферментом и снаряженных термисторами. При пропускании через измерительную колонку анализируемого образца происходит химическая реакция, которая сопровождается регистрируемым тепловым эффектом. Данный тип датчиков интересен своей универсальностью.
Заключение.
Итак, проведя анализ практического применения теплового эффекта химических реакций, можно сделать вывод: тепловой эффект вплотную связан с нашей повседневной жизнью, он подвергается постоянному исследованию и находит всё новые применения на практике.
В условиях развития современных технологий теплой эффект нашел свое применение в различных отраслях. Химическая, военная, строительная, пищевая, горнодобывающая и многие другие отрасли используют тепловой эффект в своих разработках. Он применяется в двигателях внутреннего сгорания, холодильных установках и в различных топочных устройствах, а также в производстве хирургических приборов, жаропрочных покрытий, новых видах строительных материалов и так далее.
В современных условиях постоянно развивающейся науке, мы наблюдаем появление всё более новых разработок и открытий в сфере производства. Это влечет за собой всё новые и новые области применения теплового эффекта химических реакций.
Список литературы
1. МусабековЮ. С., МарселенБертло, М., 1965; Centenaire de Marcelin Berthelot, 1827-1927, P., 1929.
2.Патент 852586 Российская Федерация. МКИ В 28 Д 5/00. Способ размерной обработки алмаза /А.П.Григорьев, С.Х.Лифшиц, П.П.Шамаев (Российская Федерация). - 2 с.
3.Классен В.К. Материальный баланс.Теплотехнические расчеты тепловых агрегатов. – Белгород: БТИСМ, 1978. –114 с.
4.Перегудов В.В., Роговой М.И. Тепловые процессы и установки в технологии строительных изделий и деталей.– М.:Стройиздат,1983.-416с.
5.Е-mail:gp_lab@inbox.ru
6."Биотехнологии" ().
7.С.Д. Варфоломеев,
Ю.М. Евдокимов, М.А. Островский. "ВЕСТНИК РОССИЙСКОЙ АКАДЕМИИ НАУК".