Шпоры по аналитической химии
| Загрузить архив: | |
| Файл: ref-24963.zip (48kb [zip], Скачиваний: 686) скачать |
1 Предмет и задачи АХ. Значение АХ в совр.науке. анализ в биологии и службе охраны природы.
АХ-наука о методах определения качественного и количественного состава ве-ва, АХ явл.составной частью единой хим.науки.
Предмет АХ- разработка методов анализа, их практич.выполнение, опр-е состава ве-в, изучение физ.св-в ве-в.
Задачи-1. развитие теории методов анализа.
2. разработка и совершенствование методов анализа.
3. обеспечение хим.-аналитич.контроля в процессе проведения научно-исследовательских работ.
Большое место отводится в АХ поиску новых совр.методов анализа, с использованием новых достижений науки и техники. Анализ имеет большое значение для промышленности, медицины. Определяется состав вод, почв. В пром-ти исп-ся состав как количественный так и качественный сплавов материалов и т.д.
2.Концентрация и активность. Ионная сила раствора.
Концентрацию, в завист-ти от раствора выражают след.способами5
 молярная
молярная
 эквивалентн.
эквивалентн.
Т-титр.
Если использумые ве-ва явл.электролитами, то их состояние хар-ся степенью диссоциации L.
Активность- та эффективная кажущаяся концентрация ионов в р-ре, в соотношении с кот.он проявляет себя в химич.реакции
Активность связана с концентрацией в соотношении: a=f*c, где f- коэф-т активности.
Значение коэф-та активных ионов опр-ся только ионной силой раствора, и не зависит от природы других ионов, присутствующих в растворе- закон ионной силы Льюиса и Рэндала.
Ионная сила при этом хар-т общее содержание ионов в растворе и рассчитывается как

3 Хим.равновесие. константа хим.равновесия (концентрационная, термодинамическяа, условная). Равновесная концентрация. Понятие об аналитич.концентрации.
Концентрация ве-в, имеющая место в системе с момента наступления равновесия, наз-ся равновесными [] . эти концентрации остаются неизменными столько долго, сколько не изменяется внешнее условие.
Равновесная концентр.ве-ва зависти от его исходной концентрации ве-ва и расхода ве-ва на протекание р-ции до момента установления равновесия.

т.о аналитич.концентр.-это общая концентрация ве-ва в р-ре, независимо от формы его содержания (ионы, молекулы).
Для обратимых р-ции з-н действ.масс запис-ся в виде конст.равновесия А+В↔С+Д

4 Теории кислот и оснований (Аррениуса, Льюиса, Бренстеда-Лоури)
одной из первых теорий, объясняющих природу кислот и оснований явилась теория электролитич.диссоциации Аррениуса-Оствальда. Согласно ей кислотой является электронейтральное ве-во, которое при диссоциации в воде в качестве катиона обрзует только ионы водорода Н+.
НА↔Н++А-
А основанием явл.ве-во, кот.при диссоциации образует в воде в кач.аниона только гидроксид-ионы
NaOH→Na++
Но так как возникали некот.трудности (некот.ве-ва проявляли св-ва солей, кислот и т.д), то пришла на смену протолитическая теория кислот и оснований- Бренстеда-Лоури, согласно которой кислотой явл.любое ве-во, способное отдавать протон, а основанием способное принимать протон.
Многие соли в водных р-рах ведут себя как кислоты, хотя Н+ в их составе нет. Эти факты были объяснены в теории Льюиса, но она не нашла широкого применения.
5 Протолитическая теория: анализ роли растворителя. Классификация растворителей.
ТеорияБренстеда-Лоури, согласно которой кислотой явл.любое ве-во, способное отдавать протон, а основанием способное принимать протон.
Растворитель явл.не только явл.средой, но и участником процесса.
Растворители:
1. протонные-могут отдавать или принимать протон.
· Кислотные- спос-ть к отдаче протона, основные-спос-ть присоединять протон, амфотерные.
2. апротонные – не обладают донорно-акцепторными св-ми по отношении к протону.
Если ве-во взято в кач.растворителя, то в зависимости от того, какая тенденция отдача или присоединение протона у него преобладает, то оно может различным образом влиять на ионизацию растворенного ве-ва
По влиянию на кислотно-основные св-ва%: невелирующие и дифференцирующие.
6 Автопротолиз растворителей. Влияние растворителей на силу кислот и оснований.
Автопротолизу подвергаются амфотерные растворители.
Если ве-во взято в кач.растворителя, то в зависимости от того, какая тенденция отдача или присоединение протона у него преобладает, то оно может различным образом влиять на ионизацию растворенного ве-ва.
Автопротолиз растворителей протекает в незначит.степени, в р-ре наступает арвновесие кот.описывается константой:


это важнейшее выражение, свидетельствующее о том, что в любом р-ре имеются как ионы водорода, таки гидроксид ионы.
Реакция среды: рН=-lgaH+
рН=7 в нейтральном р-ре,
рН<7 в кислом
pH>7 в щелочном.
Анологично водородному опр-т гидроксильный показатель рОН= lgaОН+
А выр-е часто записывают в логарифмич.форме: рН+рОН=14
8 Равновесие в водных растворах сильных и слабых кислот и оснований. Расчет рН.
1.Когда слабые к-ты диссоциируют в незначит.степени, то в р-ре наступает равновесие.
НА↔Н++А-
Оно опис-ся 
2. сильные к-ты в водн.р-рах дисс-т практич.нацело
НА→Н++А- концентрация ионов водорода совпадает с общей конц.кислоты в р-ре, а рН=-
[H+]=Cк, рН=-lg[H+]=-lgCk
3. сильные основания (щелочи) дис-т нацело
ВОН→В++ОН-
4. слабые основания-дис-т в незначит.степени и этот процесс опис-ся соответствующей константой, и наз-ся константой диссоциации слаб.основания.
ВОН↔В++ОН-

9 Буферные р-ры. Механизм буферного действия, понятие буферной емкости. Расчет рН.
Сущ-т р-ры при + к которым небольш.кол-ва кислоты, щелочи или при их разбавлении рн изменяется незначительно- буферные р-ры. А указанная их способность поддерживать рн практически постоянной наз-ся буферным действием.
Буф.спос-тью обладают смеси след.типа:
1.смесь слабой к-ты и соли с одноименным анионом. CH3COOH+CH3COONa
2. смесь слабого основания и соли с одноименным катионом NH3+NH4Cl
3. смесь слабой многоосновной к-ты различной степени замещенности NaH2PO4+Na2KPO4
Буферное действие р-ров хар-ся буферной емкостью. Это то мин.кол-во сильной к-ты или щелочи, кот.необходимо добавить к 1 л. Буферного р-ра, чтобы его рН изменилась на еденицу.
рН буф.р-ров зависит от конст.диссоциации слабой к-ты или основания и от компонентов буф.р-ра.
[H+]= Ккисл*(Скисл./Ссоли)
[ОH-]= Косн.*(Сосн../Ссоли)
10 Равновесие в водных р-рах гидролизующих солей. Расчет рН.
Расчет рН в р-рах солей:
1) гидролиз по аниону

для расчета рН в р-ре соли удобнее ползоваться след.схемой:
а) написать Ур-е р-ции гидролиза
б) рассчитать концентрацию ионов
в) рассчитать рОН, затем рН
2) при гидролизе по катиону

3) в случае совместного гидролиза по катиону и аниону
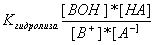
11 понятие об окислительно-восстановительной системе. Окислительно-восстановительный потенциал. Ур-е Нернста.
Признаком ОВР явл.переход электронов от одних частиц к другим.
Напр. 2Fe2++Sn2+→2Fe2++Sn4+
Электрон переходит от ионов олова (восст-ль) к ионам железа (ок-ль).
Каждую ОВР можно представить как сумму 2х полуреакций:
Восстановление- окислителя и окисление-восстановителя.
Роль окислителя закл.в присодеинении электрона, а роль восст-ля в их отдаче, то т.о различие в силе ок-ей и восст-лей связана с их спос-тью к присоединению или отдаче электрона.
Чем легче атом, ион, молекула отдает электрон , тем является более сильным восст-лем, и наоборот, чем больше средство к Эл-ну, тем более сильным окислителем она явл.
Количественно эту активность хар-т значением Е-потенциала.
ОВ систему или редоксопарузапис-т: Fe3+ /Fe2+
Sn4+ / Sn
Потенциал отдельн.редоксопар изменить невозможно, но можно составлять гальванич.эл-ты, комбинируя редоксопары с одной и той же системой, условно принятой в качестве отсчетной. Такой отсчетной системой явл.система (2Н+/Н2).
Потенциал ОВ пары зависит не только от ее природы, но и от др.факторов- гл.явл. концентрация и активность.
Ур-е Нернста: 
где, Е0 –станд. ОВ потенциал, R-газовая постоянная, T-абсолютная температура, n-число электронов участвующих в процессе, F-постоянная Фарадея (96500 Кл/моль), под log стоит отношение активности окислительных и восстановительных форм.

ЗначениеЕ наз-т реальным ОВ потенциалом системы.
12. константа равновесия ОВР.
Возможность протекания ОВР в противоположн.направлении свидетельствует о ее обратимости. Обратимые хим.р-ции хар-ся константой равновесия. ОВ потенциалы соответствующих редоксопар опр-ся Ур-ем Нернста.
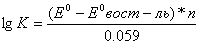
где, n- общее число электронов переходящих от ок-ля к восст-лю.
Применение ОВР в анализе многообразно: для обнаружения ионов, для количественного обнаружения ионов, разделения ионов, устранения мешающих анализу ионов.
13. комплексные соединения, их строения и типы. Внутрикомплексные соединения.
14. устойчивость комплексных соединений
15. понятие органич.реагентов. теоретические основы их действия
под органич.реагентами понимают органич.соединения, применяемые в анализе для след.целей:
1. качественное и количественное обнаружение ионов.
2. разделение ионов.
3. маскирование.
Широкое применение реагентов обусловлено их достоинствами в сравнении с неорганическими:
1. высокая селективность.
2. высокая чувствительность (опр-е малое кол-во ионов в разбавленных р-рах)
3. большое кол-во доступных реагентов и возм-ть изменения их свойств.
Впервые реагенты были предложены для применения в анализе Илинским, кот.в кач.реагента ан ионы Со предложил использовать органические.
Неск.позже Чугаевым был предложен диметилглиаксин для опр-я ионов Ni.
Св-ва органич.реагентов зависят от присутствия в их молекулах опр.атомных групп, обладающих кислотными св-ми.
Атомы водорода входящиев их состав способны замещаться атомами Ме. Кроме того в молекуле органич.реагента присутствует др.группа атомов, обладающих неподделенной электронной парой. Поэтому катион Ме одновременно образует донорно-акцепторую связь с указанным атомом.
16. классификация методов анализа. Требования к методам анализа и к результатам.
Анализ ве-в проводится для установления количественного и качественного состава ве-в.
Качественный анализ- позволяет установить, из каких эл-тов состоит ве-во.
Количественный – позволяет установить количественное содержание составных частей в анализируемой среде.
Методы м/классифицироваться в зависимости от кол-ва анализируемого ве-ва:
v Макрометоды,
v Полумикрометоды
v Микрометоды
v Ультрамикрометоды
v Субмикрометоды (очень важны в медицине, биологии).
В зависимости от техники выполнения анализа:
v Химические- в основе хим.реакция.
v Физико-химические- о составе анализируемого ве-ва судят по физ.св-ву продукта (плотность)
v Физические- судят по физическому свойству.
Четкой границы м/у физич. и физич.-хим. р-ции нет, а объединяет их то, что и там и там исследуются св-ва при пом.прибора.
17.аналитич.реакции и реагенты, требования к ним. Сп-бы повышения селективности и чувствительности
Реагент- ве-во, вызвавшее аналитическую реакцию.
Аналитические р-ции м/осуществляться двумя способами:
v Мокрым- хим.р-ция осуществляемая м/у растворами исследуемого ве-ва и реагента. Она проводится на фильтр.бумаге, предметном стекле с посследующим рассмотрением формы образовавшихся кристаллов.
v Сухим- прокаливание, пирохимические р-ции.
Хим.методы количественного анализа: гравиметрические (весовые), титриметрические (объемные).
Требования методов анализа: 1.чувствительность- определение возможно меньших количеств ве-в.
2. силективность-из большого кол-ва находящихся в образце метод д/определить одно единственное.
3. экспрессность- время затраченное на анализ д/быть минимальным
18.дробный и систематический анализ ионов, групповой реагент.
Дробный анализ- обнаружение ионов при помощи специфических раствориетлей в необходимых порциях исследуемого р-ра.
Систематический
Последовательность обнаружения ионов м/б различной.
Если специфические р-ции отсутствуют, обнаружение ионов этим методом невозможно. Разрабатывается опр.последовательность реакций обнаружения отд.ионов.
Например, р-р содержит ионы Ca2+ и Ва2+ . Чувствительной реакцией на ионы Са явл. образование осадкаCa2+ +С2О42- →СаС2О4 также и опр-т ионы ВаВа2+ +С2О42- → ВаС2О4
Значит, в присутствии Ва обнаружить СА невозможно.
В связи с многообразием ионов их обычно отделяют от р-ра не по одиночке, а целыми группами, например, добавление соляной к-ты вызывает осаждение ионов серебра, ртути. Такой реагент наз-т групповым.
Требования: 1. ионы д/осаждаться практич.полностью.
2. избыток реагента не д/мешать обнаружению остальных ионов в р-ре.
3. образ-ся осадок должен быть раст-н в кислотах.
19. подготовка образца к анализу: понятие средней пробы, ее представительность, СП-бы отбора, вскрытие.
В ходе анализа м/выделить след.этапы:
1. отбор и усреднение пробы, взятие анвески.
2. разложение пробы.
3. разделение опр.компонента.
4. количественное определение.
5. расчет результатов.
Иногда в анализа реализуются не все этапы, а некот.из них.
Однако в любом случае необходимо отобрать от образца опр.кол-во ве-ва, таким образом, чтобы рез-т анализа показывал состав всего ве-ва. Это небольшое кол-во анализируемого ве-ва, кот.по всем показателям идентично основной массе наз-ся средней пробой. Основное требование к ней представительность, т.е ее состав д/б идентичен среднему составу исследуемого образца.
Сп-бы отбора:
1. если ве-во однородно и в жидком или газообр.состоянии, его перемешивают по всему объему и отбирают небольшое кол-во для анализа.
2. твердые сыпучие ве-ва перемешивают и отбирают среднюю пробу методом «конверта», насыпают и отбирают пробу в указанных точках.
3. в тв.несыпучих ве-х образец сверлят равномерно по всему объему и для анализа берут стружку.
Вскрытие перевод всех определяемых компонентов в удобное для анализа состояние (1.мокрое- растворение пробы в подходящем растворителе- вода, кислоты,2.сухое- исп-ся когда подобрать растворитель невозможно-прокаливание, )
20. гравиметрич.метод анализа, сущность, виды. Механизм образования осадка. Условия образования кристаллич .и аморфных осадков.
Гравметрический м-д анализа- основан на точном измерении массы навески выделенной либо в чистом виде, либо в виде соединения определенного раствора.
Взвешивание произв-ся на аналитич.весах с точностью до 0,0001 гр. Результат анализа проводится с округлением до сотых 0,01 гр.
v Метод отгонки- определяемую составную часть образца отгоняют накаливанием, нагреванием.
А) прямой м-д отгонки
Б) косвенный.
Методы отгонки явл.универсальными и имеют ограниченное применение.
v Метод осаждения- определяемый эл-т переводят в труднорастворимое соединение и по массе образовавшегося осадка расчитывают его содержание, выражая это содержаниев %от массы исходного образца.
Стадии:
II. Осаждение- определяемый компонент осаждают в виде малорастворимого соединения.
III. Отделение осадка- отд.осадок от растворафильтрованием и промывают.
IV. Прокаливание- осадок высушивают или прокаливают и точно взвешивают.
V. Расчет результата- по массе осадка и его форме рассчитывают содержание в нем компонента и выражают это содержание в %.
Вид осадка зависит какот индивидуальных свойств веществ, так и от условий осаждения.
Чаще всего работают с аморфными осадками, т.к кристаллич.не всегда можно получить.
21. формы осадка, требования к ним и осадителю.
На стадии прокаливаниямногие осадки претерпеваютхим.превращение:
- Осаждаемая форма- то соединение, в виде которого определяемый ион осаждается из раствора.
- Весовая форма- то соединение, которое взвешивают для получения окончательного результата.
Опред.ион соединитель осаждаемая ф-ма весовая ф-ма
SO42- + Ba2+ → BaSO4 ↓ → BaSO4
Требования косаждаемой форме: малая растворимость, крупнокристаллическая структура осадка, возм-ть легко и полностью переходить в весовую форму.
Требования к осадителю: специфичность, летучесть.
22. загрязнение осадка, борьба с загрязнением.
Образующийся в анализе осадок практич. всегда явл.загрязненным, т.е содержит примеси посторонних веществ.
v соосаждение.
v ___________________
механизмы протеканиясоосаждения:
1. адсорбция- осаждение примесей на поверхности формирования осадка.
2. окклюзия- захват примеси внутрь осадка, при его быстрой кристаллизации.
3. изоморфизм- образование смешанных кристаллов.
4. образование хим.осаждений.
vпослеосаждение (1,3,4).
Для удаления примесей используют приемы:промывание осадка
созревание осадка
перекристаллизация
23.сущность титриметрического .метода анализа. Требования к реакциям в титриметрии. СП-бы фиксирования точки экв.
Титриметрический метод анализа основан на точном измерении объема реагента, затрачиваемого на реакцию с определяемыми ионами.

Виды титр.м-да анализа:
v кислотно-основное
v окислительно-восстановительное
v комплексо-метрическое
v осадительное.
По способу титрования: прямое, обратное, заместительное.
В ходе анализа требуется точно заметить момент наступления эквивалента, или зафиксировать точку экивалентности.
1 индикаторный- в реакц.смесь + индикатор, кот.в точке экв.меняют цвет.
2 безиндикаторный- если титрант окрашен, то добавляют или его избыток, и появляется неисчезающее окрашивание р-ра.
В титр.методе р-ции должны: протекать быстро, количественно, д/существовать возм-ть фиксировать точку эквивалентности, д/отсутствовать побочные реакции.
24.Кислотно-основное титрование, сущность метода, виды, оласть применения. Построение кривых титрования.
Относятся методы, в основе которых лежит реакция нейтрализации.
Н++ОН-→Н2О
Различают: Ацидиометрию- определение оснований, титруя их кислотами.
Алкалиметрия- щелочами.
Метод исп-ся для определения сильных и слабых кислот и оснований, солей подвергающихся гидролизу.
Характеристикой р-ра, изменяющегося в ходе кисл.-осн.титрования явл. рН.
Кривая, показывающая изменение рН р-ра, изменяющаяся в зависимости от раствора прибавленного титранта наз. Кривой кислотно-основного титрования. В основе метода лежит скачок рН.
25.кислотно-основные индикаторы. Ионно-хромофорная теория индикаторов.
Для фиксирования точки экв-ти в р-р + спец.ве-во индикатор.
К индикаторам осн.-кисл.титр-я предъявляют след.требования.
1. окраска индикатора д/б интенсивной.
2. окраска индикатора при близких значениях рН д/сильно различаться.
3. изменение окраски д/происходить в узком интервале рН.
4. изменение окраски д/б обратимым.
Титр-е предст.собой слабые органические кислоты или основания, у которых неонизированные молекулы и ионы имеют разл.окраску.
Изменение окраски инд.происходит не при всяком изменении рН, а лишь внутри опр.интервала значений рН, кот.наз. интервалом перехода индикатора.
Середина этого интервала при кот. заканчивается титрование с данным индикатором наз. его показателем титрования.
Фенолфталеин 9,0 рТ
Лакмус 7,0 рТ
Метил.красн. 5,5 рТ
Метил.оранж. 4,0 рТ.
Показатель титрования д/находится в области скачка на кривой титрования!!!
Экстракция –процесс избирательного растворения отдельных компонентов смеси ве-в в каком-либо растворителе.
27. Примеры окислительно-восстановительного титрования:перманганатометрия. Возможности метода, особенности фиксирования точки экв-ти.
Для опр-я многих неорганич.и органич.ве-в исп-т перманганат калия.
1. прямой метод титрования- когда р-ция происх.в сильно кислом р-ре.
2. косвенное- когда ионы осаждают в виде оксалатов, затем титруют перманганатом связанную с Ме щавелевую к-ту или ее избыток, введенный в р-р при осаждении.
Многие органич.ве-ва так же окисляются перманганатом, но р-ция обычно протекает медленно и исп-т косвенное титр-е.
При титр-ии перм. Обычно не используют индикаторы, т.к окраска и так достаточно выражена для установления точки эквивалентности.
Преимущества метода:
1. исходные стандартные р-ры перм.окрашены в малиновый цвет, поэтому точку экв.можно определить по цвету-прямым миетодом, или по бесцветной окраске-косвенным методом.
2. титр-е м/осуществлять в кислой или щелочной среде.
3. перм.явл.дешевым и доступным реагентом.
Недостатки:
1. исх.реагент перм.калия трудно получить в чистом виде.
2. некот.р-ции протекают при комн.темп.медленно.
3. стандартные р-ры перм.не очень устойчивы.
28. Примеры окислительно-восстановительного титрования: иодометрия. Возможности метода, особенности фиксирования точки экв-ти.
иодометрия-метод анализа, при котором о кол-ве определяемого ве-ва судят по кол-ву поглащенного или выделенного иода.
Окислитель-иод, кот.всупает в р-цию с некот.восстановителями.
J2+2e↔2J-
Опр-е иод.методом проводят как прямым, так и обратным титрованием. Кол-во выделившегося иода определяют титрованием его р-ром тиосульфата натрия.
Очень чувствительным явл.р-р крахмала.
Если к р-ру какого-либо восст-ля+ р-р иода, то в точке экв. От линии кпли иода р-р в присутствии крахмала приобретет неисчезающую синюю окраску. Но при постепенном добавлении восст-ля к р-ру иода окраска будет исчезать.
В иодометрии нужно иметь рабочий р-р иода для определения восстановителя.
29. комплексонометрическое титрование, комплексометрическое титр-е. построение кривых титрования, фиксирование точки экв-ти.
комплексонометрическое титрование основано на реакциях комплексообразования
растворы ве-в, способные образовывать комплексные соединения это титранты. Среди них исп-ся ткаие комплексообразователи, как J-, Cl-, Cr- и т.д.
В кач.титрантов исп-т растворы комплексонатов (этилен, тетроуксусная к-та и ее соли).

комплексон 2
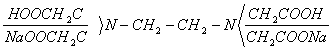
Использование комплексонов в титриметрии выделило этот СП-б титрования в отд.область комплексометрического титрования-комплексонометрическое титрование.
Осн.хар-кой р-ра явл.концентрация ионов Ме в нем.
Кривая титрования строится в координатах.
Для фиксирования точки экв.исп-ся так наз.металоиндикаторы, кот.явл.органич.красителями, образованными ионами Ме. Окрашенные комплексные соединения менее прочны, чем компл-с Ме с комплексоном.
Комплексоны не явл.спец.реагентами, поэтому увеличить силиктивность их действия, т.е определить ионы в присутствии других, можно лишь с изменением рН р-ра.
34. атомная эмиссионная спектрометрия. Качественный и количественный спектральный анализ.
атомная эмиссионная спектрометрия-физич.метод определения хим.состава ве-ва по его спектру, испускаемому возбуждаемыми атомами.
Суть метода: устройство для ввода пробы + источник возбуждения (пламя горелки). Под воздействием высоких температур растворитель испаряется, а ве-во перводится в атомароное сот-е, и атомы возбуждаются. Затем атомы возвращаются в исходное сотояние, испуская при этом избыточную энергию. Это излучение проходит ч-з диспергирующий элемент, где оно разлагается в спектр, после чего улавливаетяс фотоэлементом.
С=
Вид спектра явл.качественной хар-кой ве-ва, а интенсивность линий спектра явл.количественной хар-кой.
Т.к число линий атомов в спектре велико, то для аналитич.цепей исп-ся не все линии, а лишь некоторые из них-это так наз.аналитические линии.
35.Атомно-абсорбционная спектрометрия, сущность метода
метод основан на поглащении лучей атомами в газовой фазе, образующийся в пламени, при распылении в нем исследуемого р-ра.
Метод предполагает создание слоя поглащающего атомного пара, пропускание пучка лучей ч-з слой, разложение прошедшего потока в спектр и измерение оптич.плотности.
Концентрацию Эл-та м/находить по методу градуированного графика
36. Понятие о других спектральных методах анализа: люминесцентный, рефрактрометрический.
Люминесцентный.
В опр.условиях поглащенная атомами энергия м/выделяться в виде лучистой энергии. Люминесцентное свечение м/б вызвано действием разл. видов энергии. Свечение ве-ва м/происходить под влиянием бомбардировки его потоком электронов- катодными лучами. Такое свечение наз-ся катодо-люминисценцией, оно исп-ся в лампах дневного света. Под влиянием энергии хим.реакции м/происходить свечение, называемое химиялюминисценцией. Свечение м/б вызвано поглащением лучистой энергии- фотолюминисценция.
По хар-ру люминисцентного свечения различают фосфоросценцию (свеч.продолжающееся после удаления источника свечения) и фиуоросценцию (свеч.прекращающееся сразу же после удаления источника возбуждения свечения).
Все эти виды свечения схожи по своейприроде и объединяются общим понятием – люминисценция.
Рефрактометрический основан на определении показателя (коэф-та) преломления исследуемого ве-ва.
Если луч света переходит из одной среды в другую, то он частично отражается от поверхности раздела, а частично преломляется.
Показателемпреломления наз-т отношение sin угол падения луча света кsin угла его преломления.

37. электрохимические методы анализа, обзор, краткая хар-ка.
Основаны на взаимодействии ве-вас эл.током.
1. электровесовой- определяемыйэл-т выделяют электролизом. Хар-ся высокой точностью, применяется для определения компонентов сплавов. Недостаток-энергоемкость, непродолжительность по времени.
2. кулонометрический- основан на измерении кол-ва электричества, затраченного на р-цию с определяемым ионом. Расчеты ведутся по з-ну Фарадея.
3. кондуктометрический- основан на измерении электропроводности исследуемого р-ра.. ЭС-электропроводность опр-ся суммарным соединением всех ионов.
4. потенциометрический
5. полярографический
6. амперометрическое титрование- в кач.индикаторного электрода исп-ся полярографич.устр-во
38 потенциаметрический м-д
измерения проводят в так наз.эл.хим.ячейке, это система из 2х электродов, погруженных в исследуемый р-р и соединенных с измерительным прибором.
По роли в анализе электроды:
· индикаторный-электрод, потенциал которого зависит от концентрации определяемых ионов в исследуемом р-ре. Исп-ся в кач.электрода стеклянный, металлический э-д.
Ур-е Нернста: 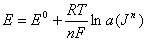
· электрод сравнения-потенциал его постоянен, независимо от протекания какой-либо р-ции в р-ре.
39. потенциаметрический м-д анализа: прямая потенциометрия и потенциометрическое титрование.
1. прямая потенциометрия-измеряют ЭДС гальв.элемента и по урю Нернста рассчитывают концентрацию определяемых ионов.
2. потенциометрическое титрование- исследуемый р-р титруют подходящим элементом, одновременно следя за изменением потенциала электрода.
Положение точки экв.опр-ся графически. Интегральная кривая
Для получения более точных рез-тов исп-т дифференциальную кривую или метод Грана
В случае прямых потенциаметрич.измерений исп-ся след.способы расчета концентрации:
1. м-д градуированного графика
2. метод прямых расчетов (ур-е Нернста)
3. метод добавок.
40 полярографический метод. Сущность, схема прибора
Основан на использовании концентрационной поляризации, возникающей в процессе электролиза, на электроде с малой поверхностью. В кач.такого исп-ся ртутный капающий электрод. Капля ртути, вытекающая из капиляра с опр.периодичностью, анодом при этом служит слой ртути на дне полярогорафич.ячейки.
Ток овнешнего источника идет на реохорд (R) , при пом. (R) на ячейку плавно подается напряжение. Пока напряжение невелико, то и потенциал не большой, и восстановление ионов на катоде не происходит. Ток ч-з ячейку практич.не идет (участок 1)
При пост.увеличении напряжения потенциал катода тоже увелич-ся, и достигает значения достаточного для восстановления ионов из р-ра. сила тока проходящая ч-з р-р резко возрастает (участок 2).
Далее при увеличении напряжения достигается такое значение потенциалакатода, при котором все ионы успевают разрядиться (участок 30.
Величина тока, протекающая ч-з раствор достигает предельного значения и наз-сядиффузионным предельным током. Т.о, зависимость напряжения имеет вид ступеньки или полярографической волны.
Если в р-ре присутств.неск.ионов, способных восстанавливаться при разл.значениях потенциала, то кол-во ступенек на полярограмме возрастает.
Ур-е полярографич.волны:

41. Полярографическая волна, качественный и количественный полярографич.анализ.
Ур-е полярографич.волны:

величина, приложенного к ячейке напряжения связанасилой, проходящей ч-з раствор тока уравнением полярографич.волны.
где, Е1/2 так называемы потенциал полуволны, явл.качественной характеристикой иона. Это то значение потенциала, при котором сила тока, протекающего ч-з раствор достигает половины величины Jдиф. (диффузионной силы тока).
Количественной хар-кой явл.высота полярографической волны, или величина предельного Jдиф., которая прямо пропорциональна концентрации ионов.
43. Экстракция –сущность метода, количественные хар-ки.
Экстракция процесс распределения растворенного вещества между двумя несмешивающимися жидкими фазами и основанное на этом выделение и разделение веществ.
Процесс экстракции характеризуют следующими основными величинами;
константа экстракции, константа распределения Р, коэффициент распределения Е, степень извлечения R, фактор разделения S.
Разделение веществ методом экстракции основано на различной растворимости их в несмешивающихся растворителях. Если какое-либо вещество способно растворяться в двух несмешивающихся растворителях, например в воде и в каком-нибудь органическом растворителе, то оно распределяется между этими двумя растворителями и устанавливается равновесие:
Авода↔Ар-тель
По закону распределения, если распределяемое вещество в обеих фазах находится в одной и той же форме, то концентрации его в этих фазах связаны зависимостью:
[Ар-тель]/[ Авода] = E
где Е - коэффициент распределения.
Коэффициент распределения зависят от температуры, свойств вещества и свойств фаз. Зависимость коэффициента распределения от температуры может быть самой разнообразной. В одних случаях с повышением температуры коэффициент распределения увеличивается — экстрагирование улучшается, в других коэффициент распределения уменьшается — экстрагирование ухудшается.
Метод экстр.очень прост и эффективен. В делительной воронке встряхивают исследуемы р-р с органическим растворителем и после расслоения жидкостей выливают их последовательно из воронки. С пом.этого метода можно извлекать ве-ва из очень разбавленных растворов.
44.Хроматография –теоретич.основы, классификация методов.
Хроматография - это физико-химический метод разделения и анализа смесей газов, паров, жидкостей или растворенных веществ сорбционными методами в динамических условиях. Метод основан на различном распределении веществ между двумя несмешивающимися фазами - подвижной и неподвижной.
Подвижной фазой может быть жидкость или газ, неподвижной фазой - твердое вещество, которое называют носителем.
Таким, образом, хроматографию можно определить как процесс, основанный на многократном повторении актов сорбции и десорбции вещества при перемещении его в потоке подвижной фазы вдоль неподвижного сорбента.
Хроматографический метод анализа разработан русским ботаником М.С.Цветом в 1903 г. С помощью этого методаон разделил хлорофилл растений на неск.веществ.
Различные методы хроматографии можно классифицировать:
По агрегатному состоянию фаз различают жидкостную и газовую хроматографию.
Разделение веществ протекает по разному механизму, в зависимости от природы сорбента и веществ анализируемой смеси.
По механизму взаимодействия вещества и сорбента различают сорбционные методы, основанные на законах распределения (адсорбционная, распределительная, ионообменная хроматография и др.), гельфильтрационные (проникающая хроматография), основанные на различии в размерах молекул разделяемых веществ.
По технике выполнения хроматографию подразделяют на колоночную, когда разделение веществ проводится в специальных колонках, и плоскостную: тонкослойную и бумажную. В тонкослойной хроматографии разделение проводится в тонком слое сорбента, в бумажной - на специальной бумаге.
В соответствии с режимом ввода пробы в хроматографическую систему различают фронтальную, элюентную и вытеснительную хроматографию.
В вытеснительном методе после введения пробы и предварительного разделения слабоактивным элюентом состав элюента меняется таким образом, что он взаимодействует с неподвижной фазой (НФ) каждого из компонентов анализируемой смеси. Вследствие этого новый элюент вытесняет компоненты, которые выходят из колонки в порядке возрастания взаимодействия с НФ. В этом методе не достигается достаточно полное разделение из-за частичного перекрывания зон.
Наибольшее распространение получил элюентный режим хроматографирования, позволяющий получать в чистом виде все компоненты пробы
45.Сп-бы проведения хроматографич.анализа, вид выходных кривых. Проявительный СП-б: качественный и количественный хр.анализ.
46. Другие виды хроматографии.
В газовой хроматографии (ГХ) в качестве ПФ используют инертный газ (азот, гелий, водород), называемый газом-носителем. Пробу подают в виде паров, неподвижной фазой служит или твердое вещество - сорбент (газо-адсорбционная хроматография) или высококипящая жидкость, нанесенная тонким слоем на твердый носитель (газожидкостная хроматография).
Ионообменная хроматография (ИХ) является разновидностью жидкостной хроматографии и в аппаратурном оформлении ничем не отличается от других видов жидкостной колоночной хроматографии. В основе ионообменной хроматографии лежит процесс обмена между ионами анализируемого раствора (ПФ) и подвижными ионами того же знака ионообменника (НФ).
В качестве ионообменников или ионитов обычно используют синтетические полимерные вещества, называемые ионообменными смолами. Они состоят из матрицы (R) и активных групп, содержащих подвижные ионы.
Ионообменную хроматографию применяют для разделения фенолов, карбоновых кислот, оснований. Часто иониты используют для предварительного разделения сложных смесей на менее сложные. На ионном обмене основано получение ионитного молока для детского питания. Ионный обмен используют для очистки натуральных соков от ионов тяжелых металлов. Ионообменные смолы применяют для получения ионообменных мембран.
Гельпроникающая хроматография (ГПХ) представляет собой метод разделения молекул, основанный на различии из размеров.
В качестве НФ в ГПХ используют частицы, имеющие определенные размеры пор. Это различного рода гели (мягкие, полужесткие и жесткие). В качестве ПФ служат водные или органические элюенты.
Т. о., при помощи ГПХ можно разделить смеси веществ в зависимости от размеров их молекул. Так можно разделить полипептиды, белки и другие макромолекулы.
Гельпроникающая хроматография на колонке используется для очистки пестицидов, а также жирорастворимых витаминов перед их определением методом ВЖХ
По механизму разделения различают распределительную, адсорбционную, осадочную и другие виды бумажной хроматографии (БХ). В распределительной жидкость-жидкостной хроматографии бумага, приготовленная из специальных сортов хлопка, выполняет роль носителя неподвижной жидкой фазы (НФ), в качестве которой часто выступает вода, адсорбированная парами бумаги. В таком случае гидрофильная бумага используется для нормально-фазовой хроматографии.
Растворителями (ПФ) являются спирты (метанол, этанол, н-пропанол, бутанол), простые эфиры (этиловый, метиловый), кетоны (ацетон, ацетил-ацетон), эфиры органических кислот (метилацетат, этилацетат), пиридин, хлороформ. Чаще используются смеси растворителей
Тонкослойная хроматография (ТСХ) является одним из наиболее простых и эффективных экспресс-методов разделения и анализа веществ в пищевых продуктах, биологических жидкостях и других объектах, не требующих сложного оборудования. В то же время метод обладает высокой избирательностью и чувствительностью (низким пределом обнаружения). Этим методом можно определить 10-20 мкг вещества с точностью до 5-7%.
В зависимости от природы НФ тонкослойная хроматография может быть адсорбционной и распределительной. Наиболее широко применим в ТСХ первый вариант разделения.
Хроматографическое разделение смеси на колонке вследствие медленного продвижения ПФ занимает много времени. Для ускорения процесса хроматографирование проводят под давлением. Этот метод называют высокоэффективной жидкостной хроматографией (ВЖХ)
Модернизация аппаратуры, применяемой в классической жидкостной колоночной хроматографии, сделала ее одним из перспективных и современных методов анализа. Высокоэффективная жидкостная хроматография является удобным способом разделения, препаративного выделения и проведения качественного и количественного анализа нелетучих термолабильных соединений как с малой, так с большой молекулярной массой.