Автоматическая линия цинкования в барабанах
| Загрузить архив: | |
| Файл: 023-0057.zip (1733kb [zip], Скачиваний: 226) скачать |
СОДЕРЖАНИЕ.. PAGEREF _Toc499278531 h 5
1 ВВЕДЕНИЕ.. PAGEREF _Toc499278532 h 7
2 ИСХОДНЫЕ ДАННЫЕ К ПРОЕКТУ. PAGEREF _Toc499278533 h 9
2.1 Годовая программа. PAGEREF _Toc499278534 h 9
2.2 Характеристика детали. PAGEREF _Toc499278535 h 10
3 ТЕХНОЛОГИЧЕСКАЯ ЧАСТЬ.. PAGEREF _Toc499278536 h 11
3.1 Характеристика покрытия. PAGEREF _Toc499278537 h 11
3.2 Выбор и обоснование способа нанесения покрытия. PAGEREF _Toc499278538 h 14
3.3 Выбор и обоснование типа и состава электролита для нанесения покрытия PAGEREF _Toc499278539 h 17
3.4 Обоснование режимов процесса нанесения цинкового покрытия PAGEREF _Toc499278540 h 22
3.5 Подготовительные операции. PAGEREF _Toc499278541 h 25
3.5.1 Обезжиривание. PAGEREF _Toc499278542 h 25
3.5.2 Активация. PAGEREF _Toc499278543 h 28
3.6 Заключительные операции. PAGEREF _Toc499278544 h 31
3.6.1 Пассивирование. PAGEREF _Toc499278545 h 31
3.6.2 Сушка. PAGEREF _Toc499278546 h 32
3.6.3 Промывка. PAGEREF _Toc499278547 h 33
3.7 Технологическая карта. PAGEREF _Toc499278548 h 36
3.8 Технологические инструкции по выполнению технологических процессов PAGEREF _Toc499278549 h 42
3.8.1 Сырьё и материалы.. PAGEREF _Toc499278550 h 42
3.8.2 Приготовление и корректировка электролитов. PAGEREF _Toc499278551 h 43
3.8.3 Контроль качества покрытия. PAGEREF _Toc499278552 h 44
3.8.4 Дефекты и их устранение. PAGEREF _Toc499278553 h 46
3.8.5 Анализ электролитов. PAGEREF _Toc499278554 h 47
3.8.6 Обслуживание электролитов. PAGEREF _Toc499278555 h 50
3.9 Утилизация цинка из промывных вод и очистка сточных вод. PAGEREF _Toc499278556 h 52
4 РАСЧЁТНАЯ ЧАСТЬ.. PAGEREF _Toc499278557 h 56
4.1 Выбор основного типа оборудования. PAGEREF _Toc499278558 h 56
4.2 Конструктивный расчёт основного оборудования. PAGEREF _Toc499278559 h 57
4.3 Электрический расчёт электрохимических ванн. PAGEREF _Toc499278560 h 63
4.4 Тепловой расчёт. PAGEREF _Toc499278561 h 66
4.4.1. Тепловой расчет нагревающихся ванн. PAGEREF _Toc499278562 h 66
4.4.2 Расчёт змеевика. PAGEREF _Toc499278563 h 69
4.4.3 Укрупнённый тепловой расчёт ванн. PAGEREF _Toc499278564 h 71
4.5 Материальные расчёты.. PAGEREF _Toc499278565 h 72
4.5.1 Расчёт расхода воды на промывку. PAGEREF _Toc499278566 h 72
4.5.2 Расчёт расхода химикатов и анодов. PAGEREF _Toc499278567 h 73
4.6 Расчёт вытяжной вентиляции. PAGEREF _Toc499278568 h 77
5 Охрана труда и техника безопасности. PAGEREF _Toc499278569 h 79
6 БИБЛИОГРАФИЧЕСКИЙ СПИСОК. PAGEREF _Toc499278570 h 83
1 ВВЕДЕНИЕ
Коррозия металлов, то есть разрушение вследствие электрохимического или химического воздействия среды, причиняет народному хозяйству огромный вред. Ежегодно из-за коррозии выбывает из строя свыше 35% всего вырабатываемого металла.
Для снижения потерь металла и предохранения изделий от коррозии наряду с использованием химически стойких материалов широко применяются различные виды защитных покрытий.
Помимо покрытий, предназначенных для защиты основного металла от атмосферной коррозии, различают защитно-декоративные покрытия, которые не только должны защищать металл от коррозии, но и сообщать его поверхности красивый, часто блестящий вид на протяжении определённого периода эксплуатации в атмосферных условиях.
Довольно широкое применение имеют износостойкие покрытия, назначение которых сводится к повышению сопротивления трущихся поверхностей механическому износу. Эти покрытия повышают срок службы трущихся поверхностей, в частности, цилиндров двигателей внутреннего сгорания автомобилей и других двигателей.
Покрытия из металлов и сплавов сообщают поверхности оптические, магнитные, антифрикционные и другие свойства. В последнее время покрытия из драгоценных металлов применяют всё в больших количествах в электронной промышленности – в производстве полупроводниковых приборов и различного рода электрических контактов, когда наряду с химической стойкостью требуется сообщить поверхности высокую электропроводность, низкое и постоянное переходное электросопротивление и целый ряд других свойств.
Гальванические покрытия по механическим свойствам, чистоте, коррозионной стойкости и экономичности одни из самых лучших. Возможность регулировать толщину слоя изменением продолжительности процесса и плотности тока, возможность уменьшать количество цветных металлов, расходуемых на покрытие поверхности, делают этот метод довольно привлекательным.
Гальванические процессы осуществляются в цехах защитных покрытий. Повышение технического уровня цехов защитных покрытий, внедрение современных технологических процессов и средств автоматизации способствует повышению эффективности труда и значительному увеличению производительности труда.
2 ИСХОДНЫЕ ДАННЫЕ К ПРОЕКТУ
2.1 Годовая программа
 |
На линию покрытия поступает деталь шуруп с потайной головкой А5·40 выполненный в соответствии с ГОСТ 1145-70. Данная деталь изготовлена из низкоуглеродистой стали ст3. Эскиз детали изображён на рисунке 2.1.
Рисунок 2.1 - Эскиз детали шуруп А5·40
Годовая программа составляет 50000 м2 в год.
2.2 Характеристика детали
Деталь шуруп изготавливается из стального прутка диаметром девять миллиметров на токарном станке путём удаления излишков металла при помощи различных резцов.
Термообработке деталь не подвергается. После изготовления детали защищаются от коррозии путём нанесения консервационного масла. В таком виде шурупы отправляются на склад, откуда далее подаются в гальванический цех на покрытие.
Масса одного шурупа А5·40 составляет 3,6 грамм. Габаритные размеры 8,5×8,5×40 мм. Площадь поверхности равна 0,002 м2. Шероховатость поверхности находится в пределах от Rz40 до Rz80 (см. рис. 2.1).
Шуруп предназначен для эксплуатации в климатическом районе УХЛ (по ГОСТ 15150-69). В данную комбинацию входят следующие типы макроклиматов: очень холодный (кроме Антарктиды), холодный, холодный умеренный, тёплый умеренный, тёплый сухой, мягкий тёплый сухой. Рабочая температура воздуха при эксплуатации составляет от 40 до минус 60°С.
Изделие изготавливается по третьей категории (по ГОСТ 15150-69): для эксплуатации в закрытых помещениях с естественной вентиляцией без искусственно регулируемых климатических условий, где колебания температуры и влажности воздуха и воздействие песка и пыли существенно меньше, чем на открытом воздухе, например, в металлических с теплоизоляцией, каменных, бетонных, деревянных помещениях.
3 ТЕХНОЛОГИЧЕСКАЯ ЧАСТЬ
3.1 Характеристика покрытия
Цинк – металл светло-серого цвета, отличающийся хрупкостью и сравнительно малой твёрдостью (50-60 единиц по Бринелю). Цинк обладает следующими физико-химическими свойствами: плотность 7,2 г/см3, атомный вес 65,38; валентность 2; стандартный потенциал по отношению к нормальному водородному электроду составляет минус 0,76 В; электрохимический эквивалент 1,22 г/А·ч; температура плавления 419°С; при нагреве до 100 – 150°С цинк становится пластичным и может подвергаться прокатке и ковке, при 200°С и выше цинк снова теряет пластичностьи делается настолько хрупким, что его легко можно превратить в порошок. В сухом воздухе цинк устойчив. Во влажном воздухе и пресной воде он покрывается белой плёнкой углекислых и окисных соединений, защищающих его от дальнейшего разрушения.
В морской воде цинк обладает умеренной устойчивостью. Скорость коррозии цинка в воде при различных температурах связана с изменением свойств продуктов его коррозии: при низких (20–40°С) и высоких (выше 90°С) температурах цинк покрывается плотными, прочно пристающими к нему продуктами коррозии, которые, однако, в определённом интервале температур (50–80°С) становятся рыхлыми и легко отстают от поверхности.
Цинк быстро разрушается кислотами и щелочами и легко реагирует с сероводородом и сернистыми соединениями, поэтому в таких средах цинковые покрытия неприменимы.
В кислотах цинк растворяется с выделением водорода. Примеси ртути и свинца с высоким значением перенапряжения водорода не оказывают существенного влияния на скорость растворения цинка, в то время как примеси меди, олова и других электроположительных металлов, на которых перенапряжение водорода незначительно, повышают скорость растворения цинка в кислых средах.
Основными областями применения цинковых покрытий являются: защита от коррозии деталей машин, крепежа, стальных листов, проволоки и деталей ширпотреба, работающих вне помещений, в различных климатических районах, а также в закрытых помещениях с умеренной влажностью и в помещениях, загрязнённых газами и продуктами сгорания; защита изделий из чёрных металлов от коррозии в атмосфере, загрязнённым сернистым газом, и от коррозионного воздействия бензина и масла; защита водопроводных труб, питательных резервуаров и предметов домашнего обихода из чёрных металлов, соприкасающихся с водой.
Широкое распространение цинковых покрытий в гальванической практике для защиты от коррозии изделий из чёрного металла объясняется их высокими защитными свойствами. Потенциал цинка отрицательнее потенциала чёрных металлов (стали, железа, чугуна), т. е. цинк для указанных выше металлов является анодным покрытием и защищает их от коррозии электрохимически. Защитные свойства таких покрытий сохраняются даже при малой толщине слоя, а также при наличии в нём пор или обнажённых участков.
Важную роль играет также низкая стоимость цинка по сравнению со многими цветными металлами.
Скорость разрушения цинкового покрытия составляет примерно 1,0–1,5 мкмгод для местности, характеризующейся наличием в атмосфере значительных количеств сернистого и углекислого газов.
Значительное уменьшение скорости разрушения цинковых покрытий достигается специальной обработкой их в растворах солей хромовой кислоты, а также за счёт фосфатных и оксидных плёнок, образующихся в результате применения химических и электрохимических видов обработки цинкового покрытия.
Цвет покрытия (по ГОСТ 9.301-86) серебристо-белый или серебристо-серый с голубоватым оттенком. Допускаются незначительные радужные оттенки, если нет особых требований к декоративным свойствам покрытия. Детали с цинковым покрытием не являются бракованными если:
1)матовая поверхность после гидропескоструйной и металлпескоструйной очистки, галтования, травления;
2)потемнение или ослабление интенсивности цвета хроматного покрытия на деталях после термообработки;
3)более тёмный или более светлый оттенок хроматного покрытия в отверстиях и пазах, на внутренних поверхностях и вогнутых участках деталей сложной конфигурации, острых кромках, углах;
4)матовые полосы вокруг отверстий;
5)единые механические повреждения хроматного покрытия не более 2% общей площади;
6)изменение интенсивности цвета или потемнения после прогрева с целью обезводороживания и проверки прочности сцепления.
3.2 Выбор и обоснование способа нанесения покрытия
Практическое применение находят следующие способы нанесения цинковых покрытий:
1)погружение изделий в расплавленный цинк (горячий способ);
2)метод термической диффузии;
3)металлизация распылением металлом из пульверизатора;
4)контактный метод осаждения цинка;
5)электролитический метод.
Горячий способ покрытия заключается в том, что изделия погружают в ванну с расплавленным металлом или же нагретую поверхность деталей натирают расплавленным металлом.
К недостаткам этого способа следует отнести неравномерность толщины слоя и большой расход металла. Этот способ непригоден для деталей со сложной формой и резьбой.
Диффузионный способ нанесения основан на диффузии в поверхностные слои деталей какого-либо металла при высокой температуре. Диффузионные покрытия наносят при нагреве деталей в твёрдой (порошкообразной), жидкой или газообразной фазе металла.
Способ металлизации распылением заключается в нанесении на поверхность деталей слоя металла распылением расплавленного металла.
Способ контактного осаждения осуществляется без применения внешнего источника тока, за счёт вытеснения менее благородными металлами более благородных из растворов их солей. Толщина таких покрытий, как правило, невелика и защитные свойства их невысоки.
Электролитический метод цинкования. Хотя цинк в ряду напряжений стоит немного левее водорода (Е°= –0,76 В), однако осаждение его не встречает затруднений, что объясняется высоким значением перенапряжения выделения водорода на цинке. Благодаря этому в обычных условиях электролиза водород на катоде выделяется в незначительных количествах, и ток в основном расходуется на осаждение цинка.
Основными преимуществами электролитического метода цинкования являются:
1)высокая степень чистоты электролитически осаждённого цинка, зависящая главным образом от чистоты анодов и химикатов, применяемых для составления ванн;
2)высокая химическая стойкость цинковых покрытий, полученных электролизом, обусловленная чистотой осадка;
3)малый расход цинка, обусловленный возможностью точного регулирования количества отлагаемого цинка и толщины покрытия;
4)хорошие механические свойства покрытия (эластичность покрытия и хорошая сцепляемость с основой).
Цинковые покрытия, полученные электролитическим способом, отличаются также достаточно высокой стойкостью против коррозии в условиях тропического климата.
Как видно из вышенаписанного, электролитический метод нанесения цинкового покрытия является наиболее удовлетворяющим требованиям, которые предъявляются к покрываемой детали.
Так как на деталь необходимо нанести защитно-декоративное покрытие, то по ГОСТ 9.303-84 минимальная толщина покрытия должна составлять 6 мкм, а максимальная 9 мкм.
В таком случае будет наноситься цинковое покрытие Ц6.хр.бцв. со следующими свойствами (по ГОСТ 9.303-84):
1)Цинковое покрытие является анодным по отношению к стали ст3, и защищает её от коррозии до температуры 70 °С, при более высоких температурах – механически. Покрытие предотвращает контактную коррозию стали ст3 при сопряжении с деталями из алюминия и егосплавов; обеспечивает свинчиваемость резьбовых деталей.
2)Для повышения коррозионной стойкости цинковое покрытие хроматируют. Хроматирование одновременно улучшает декоративный вид покрытия. Хроматная плёнка механически непрочная.
3)Цинковое хроматированное покрытие теряет свой декоративный вид при условии периодического механического воздействия (прикосновение инструмента, рук и т. д.)
4)Электрохимическое цинкование вызывает потерю пластичности стали в результате её наводораживания. Стали с пределом прочности более 1380 МПа (140 кгс/мм2) цинкованию не подлежат.
5)Покрытие обладает прочным сцеплением с основным металлом, низким сопротивлением механическому истиранию и повышенной хрупкостью при температуре выше 250°С и ниже минус 70°С. покрытие обладает низкой химической стойкостью к воздействию продуктов, выделяющихся при старении органических материалов.
6)Микротвёрдость покрытия в среднем составляет 490–1180 МПа (50–120 кгс/мм2); удельное сопротивление при 18°С составляет 5,75·10-8 Ом·м.
3.3 Выбор и обоснование типа и состава электролита для нанесения покрытия
Для цинкования применяют три типа электролитов: кислые, щелочные цианистые и щелочные нецианистые (цинкатные).
Во всех этих электролитах цинк находится в виде двухвалентных ионов.
Из кислых электролитов цинк выделяется в результате разряда на катоде двухвалентных ионов цинка:
ZnSO4 = Zn2+ + SO42-, (3.1)
Zn2+ + 2e = Zn. (3.2)
На разряд ионов цинка расходуется почти весь ток, так как выделение водорода ничтожно мало. Убыль ионов цинка из растворов компенсируется растворением анодов. Последнее протекает без выделения кислорода.
Протекание указанных электродных процессов на практике несколько нарушается из-за присутствия в электролите примесей, выделение которых наряду с выделением водорода несколько снижает катодный выход по току.
Кроме того, наряду с чисто электрохимическим растворением анодов происходит частичное химическое растворение цинка благодаря присутствию в растворе некоторого количества свободной кислоты.
Оба эти процесса – разряд посторонних катионов и химическое растворение анодов – изменяют коэффициенты использования тока на электродах и требуют периодической корректировки электролита.
Рассеивающая способность кислых электролитов весьма низкая.
Сульфатный электролит содержит (г/л):
ZnSO4·7H2O……………………………..……………………..……..200-300
Al2(SO4)3·18H2O……………………………………………………..………30
Na2SO4·10H2O………………………..……….…….…………………50-100
Блескообразующая добавка…………………….………………………1-5
Процесс ведётся при 18–25°С и при рН=3,5–4,5. Плотность тока в перемешиваемых ваннах составляет от 2 до 10 А/дм2 и выше.
Сульфатные ванны, несмотря на целый ряд преимуществ (устойчивость в работе, высокий выход металла по току, отсутствие в составе электролита ядовитых веществ), применяются главным образом для цинкования изделий простой конфигурации (листов, ленты, проволоки и т. п.)
Основным компонентом цианистых цинковых электролитов является комплексная соль Na2[Zn(CN)4]. Диссоциация этой соли происходит по уравнению
Na2[Zn(CN)4] Û 2Na+ + Zn(CN)42-. (3.3)
Таким образом, цинк в растворе находится в составе аниона.
Разряд на катоде требует значительной энергии активации; этим объясняется высокая поляризация, сопровождающая осаждение цинка из цианистых электролитов, и мелкокристаллическая структура покрытий.
Осаждение цинка из растворов цианистого комплекса, содержащих избыток свободного цианида, протекает при потенциале минус 1,7 В. Поэтому, несмотря на высокое водородное перенапряжение на цинке, выход по току цинка небольшой.
Потенциал осаждения цинка может быть снижен до минус 1,4 В введением в раствор свободной щёлочи. Одновременно снижается концентрация ионов водорода. Вход по току достигает 95–99%.
Цианистое цинкование при плотностях тока до 5-6 А/дм2. Осадки цинка получаются плотными, весьма тонкокристаллическими, а электролит обладает высокой рассеивающей способностью.
Характерная особенность анодного процесса при цинковании в цианистых электролитах заключается в склонности цинковых анодов к пассивированию и, следовательно, к уменьшению концентрации цинковой соли в ванне, что проявляется особенно заметно при недостатке в электролите свободного цианида. Этим объясняется непостоянство состава цианистого электролита.
Другой причиной является то, что цинковые аноды подвержены химическому растворению в цианистом калии и щёлочи. Это приводит к накапливанию цинка в электролите. Третья причина непостоянства состава электролита цианистых ванн – взаимодействие с углекислотой воздуха (по этой причине нельзя применять перемешивание).
Состав цианистого электролита имеет такой вид (г/л):
ZnO……………………………………………………………………..…40-45
NaCN…………………………………………………………..………….80-85
NaOH………………………...…………………………………………...40-60
Электролиз ведут при 18–40°С. Катодная плотность тока 1–4 А/дм2 и выход по току 70–80%.
Основной недостаток цианистых электролитов заключается в их токсичности (выделяющаяся синильная кислота – сильный яд), поэтому они применяются в редких случаях.
Цинкатные электролиты очень просты по составу. В основном они содержат цинк в виде цинката и едкую щёлочь.
Выход металла по току в цинкатных электролитах близок к 100% и мало меняется с изменением условий электролиза. Осадки, полученные из цинкатных электролитов, имеют крупнокристаллическую структуру и отличаются неравномерной толщиной слоя. Это связано с малой катодной поляризацией.
Улучшение качества осадков, полученных из цинкатных ванн, достигается добавлением в электролит небольших количеств солей олова, свинца и ртути (это способствует растворению цинка).
2 Zn + Sn4+ ® 2 Zn2+ + Sn. (3.4)
Рассеивающая способность цинкатных ванн в присутствии солей указанных металлов и при низкой плотности тока достаточно высока.
Примерный состав цинкатного электролита (г/л):
ZnO……………………………………………………………….……..…5-50
NaOH……………………………………………………...…….……...65-220
Na2SnO3……………………………………………………….....…….0,2-0,5
Процесс ведут при 50–70°С. Катодная плотность тока 0,5–4 А/дм2. выход по току 96–98%.
Сравнение достоинств и недостатков для различных типов электролитов цинкования можно наглядно увидеть в таблице 3.1.
Исходя из общей суммарной оценки, можно сделать вывод, что цинкатный электролит цинкования является самым пригодным для покрытия детали шуруп А5·40.
Таблица 3.1 – Сравнительная характеристика электролитов цинкования.
|
Свойства электролитов |
Оценочная шкала |
Высокоцианистые |
Малоцианистые |
Цинкатные |
Кислые |
Аммикатные |
|
Положительные Рассеивающая способность Выход по току Предельно допустимая концентрация Способность крыть чугун Неприхотливость в подготовке поверхности Устойчивость к температуре Лёгкость очистки сумма |
10 5 5 3 10 5 5 |
10 4 3 1 10 5 3 36 |
8 3 1 1 7 3 4 27 |
8 3 1 1 5 2 5 25 |
2 5 5 3 2 2 2 21 |
7 5 5 3 2 2 2 26 |
|
Отрицательные Агрессивность к стали Токсичность Затраты на нейтрализацию Водородная хрупкость Стоимость эксплуатации сумма |
-5 -5 -10 -5 -3 |
-1 -5 -10 -5 -3 -24 |
-1 -5 -5 -5 -2 -18 |
0 -1 -1 -3 -1 -6 |
-5 -1 -1 -1 -1 -9 |
-5 -1 -2 -1 -2 -11 |
|
Общая суммарная оценка |
12 |
9 |
19 |
12 |
15 |
3.4 Обоснование режимов процесса нанесения цинкового покрытия
При электрохимическом осаждении цинка на катоде протекает следующий процесс:
Zn(OH)42- + 2e ® Zn + 4 OH- . (3.5)
Побочным процессом на катоде является разряд ионов водорода:
2 H2О + 2e®H2 + 2 OH- . (3.6)
Выделяющийся водород в атомарном состоянии проникает в кристаллическую решётку покрываемого металла, тем самым, повышая его хрупкость. Этот процесс носит название наводораживание. Для того чтобы снизить наводораживание необходимо поддерживать высокий выход по току цинка.
Температура ведения процесса покрытия детали составляет 20-30°С. Оптимальной температурой является температура, равная цеховой (при условии, что она попадает в этот интервал), так как в этом случае отпадает необходимость подогревать ванну покрытия. При повышении температуры будет снижаться перенапряжение выделения водорода на катоде, это приведёт к большему его выделению, а, следовательно, к уменьшению выхода по току цинка и наводораживанию детали. При понижении температуры будет падать электропроводность раствора электролита, что повлечёт за собой увеличение напряжения на ванне и перерасходу электроэнергии идущей на процесс покрытия.
Для деталей сложной формы и во вращательных установках применяется катодная плотность тока в интервале от 0,5 до 1,5 А/дм3. Оптимальной будет являться катодная плотность тока, равная 1 А/дм3, так как при данной плотности тока скорость осаждения цинка будет в пределах 0,1–0,3 мкм/мин. При снижении данной плотности тока будет происходить снижение производительности и как следствие этого, повышение себестоимости детали. Кроме того, будет снижаться выход по току цинка, а это повлечёт наводораживание детали. При увеличении катодной плотности тока будет происходить рост концентрации окиси цинка (влияние см. ниже); может быть достигнут предельный ток, и будет происходить дендритообразование; будет происходить разогрев раствора электролита, а, следовательно, снижение выхода по току цинка и наводораживание детали.
Оптимальная концентрация окиси цинка в электролите составляет 10 – 17 г/дм3. При понижении содержания окиси цинка будет происходить уменьшение катодной плотности тока и снижение производительности. При повышении содержания окиси цинка будет снижаться содержание щёлочи в электролите, благодаря этому снижению будет падать выход по току цинка.
Оптимальное содержание щёлочи в электролите составляет 90– 120 г/дм3. Если содержание щёлочи будет выше, то будет происходить снижение рассеивающей способности электролита, это приведёт к ухудшению качества покрытия. Если содержание щёлочи будет заниженным, то снизится выход по току, а это повлечёт за собой наводораживание детали и снижение производительности процесса.
Оптимальное содержание блескообразующих добавок НБЦ-0 и НБЦ-К составляет 4-6 г/дм3. Повышение содержания не имеет экономического смысла, а снижение приведёт к ухудшению качества покрытия.
На основании вышеизложенного и руководствуясь информационными данными ГОСТ 9.305-84, выбираем состав цинкатного электролита для нанесения цинкового покрытия и режимы технологического процесса:
Окись цинка………………………………………………..10-17 г/дм3
Едкий натр технический марка ТР…………...……….90-120 г/дм3
Блескообразующие добавки:
НБЦ-0…………………………………………………..4-6 г/дм3
НБЦ-К…………………………………………..………4-6 г/дм3
рН………………………………………………………………....4,5-5,8
Температура…………………………………………………..20-30°С
Катодная плотность тока……………….………………0,5-1,5 А/дм3
Анодная плотность тока…………………………………….1-2 А/дм3
3.5 Подготовительные операции
3.5.1 Обезжиривание
Химическое обезжиривание заключается в том, что жиры, представляющие собой сложные эфиры глицерина и высших жирных кислот, при воздействии щёлочи омыляются и переходят в растворимые соли, а минеральные масла при воздействии щёлочи могут образовывать эмульсию.
При химическом обезжиривании применяют разбавленные растворы щёлочи, так как концентрированные щелочные растворы обладают способностью образовывать оксидные плёнки на поверхности детали, изготовленной из стали. Кроме того, образовавшиеся при обезжиривании мыла в концентрированных растворах щёлочи не растворяются, что отрицательно сказывается на прочности сцепления покрытий. Кроме едкого натра, растворы для обезжиривания содержат легко гидролизующиеся соли щелочных металлов (углекислый натрий, тринатрийфосфат и др.). Концентрация едкого натра в растворах для обезжиривания стальных деталей обычно не превышает 100 г/л.
С целью облегчения процесса отрыва капелек масла от поверхности металла и образования эмульсии в щелочной раствор добавляют поверхностноактивные вещества, так называемые эмульгаторы.
Химическое обезжиривание производят при температуре 70–90°С, при которой омыление и процесс эмульгирования протекают более интенсивно. Продолжительность обезжиривания зависит от степени загрязнения деталей и составляет примерно от 5 до 60 мин.
Корректирование щелочного раствора в процессе работы осуществляется добавкой химикатов согласно данным анализа. Периодически в зависимости от размеров обезжиривающей ванны и количества обрабатываемых деталей щелочной раствор заменяют свежим.
Электрохимическое обезжиривание в щелочных растворах производится при помощи постоянного, а иногда и переменного тока. При постоянном токе обезжиривание осуществляется на катоде и на аноде. В процессе электролиза на поверхности детали наблюдается интенсивное выделение пузырьков газа, облегчающих отрыв капелек масла от поверхности детали, чем значительно улучшается обезжиривание.
При электрохимическом обезжиривании с увеличением поляризации уменьшается прочность сцепления масла с поверхностью электрода. Параллельно с усилением поляризации увеличивается степень смачивания водой поверхности металла.
Скорость обезжиривания деталей на аноде меньше, чем на катоде. Это объясняется тем, что в прианодном пространстве не происходит защелачивания электролита, вследствие чего процесс омыления жиров у анода происходит медленнее. Кроме того, количество выделяющегося при электролизе кислорода меньше, чем количество водорода, а пузырьки кислорода больше пузырьков водорода и меньше задерживаются на поверхности капелек масла, а поэтому и удаление масла с поверхности происходит менее интенсивно. Однако процесс катодного обезжиривания сопровождается наводораживанием.
Скорость электрохимического обезжиривания значительно выше химического. Качество обезжиривание также лучше. При электрохимическом обезжиривании пользуются в основном теми же химикатами что и при химическом, только в меньших концентрациях.
Недостаток электрохимического обезжиривания – низкая рассеивающая способность применяемых растворов, вследствие чего очистка сложнопрофилированных деталей затруднительнее.
Делая анализ вышенаписанного, и при условии того, что поверхность поступающей детали сильно зажирена консервационными маслами (см. раздел 2.2), принимаем решение: в технологических операциях по подготовке поверхности детали к покрытию использовать химическое обезжиривание как предварительную очистку от масел и электрохимическое обезжиривание на катоде для лучшей очистки от масел.
Для покрываемого металла – сталь ст3, при обработке во вращающемся барабане выбираем следующие составы и характеристики процесса обезжиривания (г/л) [18]:
1)химическое
Натр едкий технический марка ТР………………………...………20-40
Тринатрийфосфат…………………………………………………......5-15
Обезжириватель ДВ-301…………………….……………….……..….3-5
Силикат натрия растворимый………….…………………….…….10-30
Температура процесса составляет 50–70°С, время обезжиривания 2–5 мин. Допускается заменять тринатрийфосфат эквивалентным количеством пирофосфорнокислого натрия.
2) электрохимическое
Натр едкий технический марка ТР………………………...………20-40
Тринатрийфосфат…………………………………………….……...5-15
Обезжириватель ДВ-301……………………………………..……1,4-1,9
Силикат натрия растворимый………….…………………….…….10-30
Температура процесса 50–70°С, катодная плотность тока 2–8А/дм3. Время обезжиривания на катоде составляет 0,5–5,0 мин. Аноды никелевые. При образовании большого количества пены в раствор добавляют 0,03–0,05 г/дм3 эмульсии КЭ 10–21.
3.5.2 Активация
Поверхность поступающей на покрытие детали покрыта слоем оксидов, который образуется при её изготовлении (см. раздел 2.2). В состав плёнки входят: FeO, Fe2O3 и Fe3O4.
Активацией называется процесс удаления с поверхности металлических деталей тончайшего, зачастую незаметного глазу слоя окислов, которые могли образоваться в промежутках между операциями. При активации одновременно происходит легкое протравливание верхнего слоя металла и выявление кристаллической структуры металла, что благоприятствует прочному сцеплению покрытия с основой.
Для химической активации чёрных металлов применяют растворы кислот (серной, соляной). При активации могут наблюдаться два процесса: химическое растворение окислов и растворение железного подокисного слоя, которое приводит к отстаиванию и удалению окислов. Эти два процесса могут протекать одновременно; в зависимости от природы кислоты, её концентрации и температуры меняется скорость, а, следовательно, преобладание того или иного процесса.
Механизм удаления окалины в серной и соляной кислотах неодинаков. В соляной кислоте растворяются преимущественно окислы, а в серной кислоте – главным образом металлическое железо с выделением водорода, который механически разрыхляет и удаляет окалину.
Растворение стальной основы – нежелательное явление, так как приводит к излишнему расходованию кислоты, потере металла, выделению вредных испарений; при этом возможно наводораживание металла. Кроме того, поверхность металла может оказаться разъеденной и шероховатой.
В таблице 3.2 показана зависимость продолжительности травления от концентрации кислот [4]. В таблице 3.3 показана зависимость продолжительности травления от температуры [4].
Таблица 3.2 - Продолжительность Таблица 3.3 - Продолжительность
травления в зависимости от травления в зависимости от
концентрациикислот (при 20 °С) температуры
|
Концентрация кислоты в вес.% |
Продолжительность травления в мин. |
Температура кислоты в °С |
Продолжительность травления в мин. |
||||
|
в соляной кислоте |
в серной кислоте |
в соляной кислоте |
в серной кислоте |
||||
|
2 5 10 15 20 25 30 40 |
90 55 18 15 10 9 - - |
135 135 120 90 85 65 75 95 |
5% |
10% |
5% |
10% |
|
|
18 40 60 |
55 15 5 |
18 6 2 |
135 45 13 |
120 32 8 |
Данные таблицы 3.2 показывают, что при концентрации кислот примерно от 20 до 25 % наблюдается наибольшая скорость травления. Данные таблицы 3.3 показывают, что скорость травления в растворе соляной кислоты в большей степени зависит от концентрации кислоты, а в растворе серной кислоты – от температуры. Приведём сравнительную характеристику преимуществ активации в соляной и серной кислотах.
Преимущества соляной кислоты:
1)
2)
3)
4)
5)
Преимущества серной кислоты:
1)
2)
Делая анализ вышенаписанного и используя справочные данные ГОСТ 9.305-84, принимаем решение: в технологических операциях по подготовке поверхности детали к покрытию использовать для активации состав с соляной кислотой.
Активационный состав:
Кислота соляная синтетическая…………………………..50-100 г/дм3
Температура процесса цеховая (15-30°С), продолжительность травления составляет 15-45 сек. Процесс активации проводится непосредственно перед покрытием.
3.6 Заключительные операции
3.6.1 Пассивирование
Для усиления защитных свойств цинкового покрытия применяется операция пассивирования путём обработки цинковых покрытий в растворах хромовой кислоты и её солей. При этой обработке происходит частичное растворение цинка с образованием плёнки хроматов цинка и соединений трёхвалентного хрома, придающих плёнке характерные цвета побежалости радужных оттенков. Толщина плёнки составляет до 0,5 мкм. Хроматные плёнки не допускают нагрева их до температуры 62°С, так как при этом происходит дегидратация, вследствие чегоснижаются защитные и механические свойства плёнок.
Образующаяся хроматная плёнка улучшает антикоррозионные свойства цинковых покрытий. Благодаря высокой пористости, которой обладают пассивирующие плёнки, они существенно улучшают адгезионные свойства оцинкованных поверхностей, облегчая тем самым нанесение на них лакокрасочных покрытий защитного и специального назначения.
Операции пассивирования обычно предшествует операция осветления. В результате этой операции цинковое покрытие приобретает более светлый оттенок. Эти операции можно проводить в одной гальванической ванне, при условии применения специальных растворов.
Состав такого раствора, применяемого во вращательных установках на автоматических линиях, такой (г/л) [18]:
Спирт поливиниловый………………..……………………………….2-6
Соль Ликонда 25…………………………………………………..….70-75
Температура процесса цеховая (18–30°С), продолжительность пассивации составляет 0,75–1,5 мин. рН=0,5–1,2.
3.6.2 Сушка
Перед тем как детали с нанесённым на них цинковым покрытием сойдут с линии их необходимо просушить. Эта операция проводится для того чтобы при дальнейшей эксплуатации не происходила коррозия вследствие большой влажности самих деталей. Кроме того, сушка способствует улучшению сцепления недавно образованной пассивной плёнки с цинковым покрытием. Характерной особенностью процесса высушивания деталей с цинковым покрытием является то, что процесс ведётся при температуре до 60°С. Это объясняется тем, что при более высоких температурах пассивная хроматная пленка разрушается, так как при таких высоких температурах происходит дегидратация, вследствие чегоснижаются защитные и механические свойства плёнок.
Сушку деталей обрабатываемых в барабанах на автооператорных линиях сушку производится в аппарате «Сушило» с циркуляцией нагретого воздуха. Разгрузка высушенных деталей в этом аппарате производится автоматически. Температура процесса не выше 60°С, продолжительность составляет 3-10 мин [18].
3.6.3 Промывка
После каждой операции подготовки и нанесения гальванического покрытия детали следует тщательно промывать, причём особенное влияние уделять тому, чтобы в гальванические ванны не попадало даже следов обезжиривающих, травильных и активационных растворов. Загрязнения могут стать причиной ухудшения сцепления покрытия с основой, появления пятен и других нарушений нормальной работы электролита. Вода должна быть как можно меньшей жёсткости, её необходимо часто менять. В некоторых случаях применяется проточная вода, которая подаётся снизу и сливается из верхней части промывочного бака или ванны (см. рис. 3.1). Скорость смены проточной воды зависит от начальной и конечной концентрации растворов и уноса раствора деталей. Промывка проводится в течение 1-3 минут, особенно после травления, чтобы удалить из всех пор остатки кислоты и солей железа.
Качество промывки может быть улучшено перемешиванием воды сжатым воздухом, а также применением разбрызгивающих устройств и струйных установок (см. рис. 3.1). Весьма целесообразно применять обессоленную воду. В результате обработки воды ионообменным способом содержание солей в воде может быть доведено до 20-40 мг/л.
После обезжиривания детали промывают вначале горячей, затем в холодной воде. Хорошо обезжиренная поверхность должна равномерно покрываться водой.
После активации перед загрузкой в ванну детали не следует промывать в горячей воде, так как при этом поверхность деталей быстро высыхает. В данном случае это нежелательно, так как тонкая плёнка влаги препятствует контакту металла с кислородом воздуха, предохраняя его от окисления.

а) погружная проточная ванна промывки; б) двухступенчатая каскадная проточная ванна промывки; в) комбинированная ванна промывки; г) струйная ванна промывки.
Рисунок 3.1 – Виды ванн промывки
Детали с нанесённым покрытием промывают сначала в проточной холодной воде, затем в горячей, чем облегчается сушка. Промывные воды не должны содержать кислот или солей более 0,2%.
По температурному режиму промывки делятся на (ГОСТ 9.314-90): холодную (15–39°С), тёплую (40–60°С) и горячую (свыше 60°С).
Следуя тому, что изложено в этом разделе, выбираем следующие операции промывки:
1)
2) °С;
3)
4)
5) °С.
3.7 Технологическая карта
Ниже приведена технологическая карта для автоматической линии цинкования в барабанах. Заполнение данных форм производилось в соответствии с ГОСТ 3.1408-85.
3.8 Технологические инструкции по выполнению технологических процессов
3.8.1 Сырьё и материалы
Для цинкования применяются вальцованные аноды марки Ц0 и Ц1 по ГОСТ 1180-60. Вспомогательные материалы, применяемые при цинковании, приведены в таблице 3.3.
Таблица 3.3 - Материалы, применяемые при цинковании
|
Наименование материалов |
Химическое обозначение |
ГОСТ или ТУ |
|
Блескообразующие добавки НБЦ-0, НБЦ-К Едкий натр технический марка ТР Кислота соляная техническая Обезжириватель ДВ-301 Окись цинка Силикат натрия растворимый Соль Ликонда 25 Спирт поливиниловый Сульфанол НП-3 Тринатрийфосфат |
- NaOH HCl - ZnO Na2SiO3 - - - Na3PO4·12Н2О |
ТУ 6-09-4799-83 ГОСТ 2263-79 ГОСТ 857-78 ТУ 38-40835-79 ГОСТ 10262-78 ГОСТ 13079-81 ТУ 6-18-200-78 ГОСТ 10779-78 ТУ 81-509-81 ГОСТ 201-76 |
3.8.2 Приготовление и корректировка электролитов
Приготовление растворов обезжиривания. Их готовят последовательным растворением всех компонентов в тёплой воде. Твёрдый едкий натр растворяют, поместив его в герметически закрытый специальный аппарат. В приготовленный раствор добавляют поверхностно-активные вещества. Корректирование растворов проводят не реже одного раза в неделю по данным химического анализа на содержание NaOH, тринатрийфосфата и других компонентов.
Приготовление раствора для активирования. Полученную концентрированную соляную кислоту растворяют в воде до 100 г/л. При приготовлении раствора нужно кислоту приливать к воде и не в коем случае наоборот, корректировка не реже раза в неделю.
Приготовление электролита цинкования. Едкий натр растворяют в 1/10 объёма ванны, в которой готовятся растворы; к нему осторожно при непрерывном помешивании добавляют рассчитанное количество окиси цинка до полного её растворения. Затем доливают воду до 3/4 объёма ванны и полученный раствор цинката натрия с избытком едкого натра фильтруют в рабочую ванну. Все добавочные компоненты растворяют отдельными порциями в небольшом количестве воды и вводят в рабочую ванну. Электролит корректируют не реже двух раз в месяц.
Приготовление раствора хроматирования. К уже приготовленному раствору соли Ликонда 25 добавляют при постоянном помешивании поливиниловый спирт. Раствор фильтруется и помещается в гальваническую ванну. Корректировка осуществляется добавлением соли Ликонда 25 и поддержанием рН не реже одного раза в неделю.
3.8.3 Контроль качества покрытия
Качество цинковых покрытий определяют по следующим основным параметрам: внешний вид, толщина покрытия, прочность сцепления. Пористость этих покрытий обычно не контролируется, так как она, учитывая анодный характер защиты, не регламентируется.
Контроль толщины покрытия на данной линии определяется химическим капельным способом. Методом случайного избрания выбирается 5 деталей из загрузки после прохождения всех технологических операций. Далее в химической лаборатории проводится анализ следующим образом: готовится раствор 200 г/л хромовой кислоты плюс 50 г/л серной кислоты, полученный раствор по капле стекает на испытуемую деталь со скоростью 100±5 капель в минуту, а толщина покрытия определяется временем, требуемым для того, чтобы обнажился основной металл. Кривые, связывающие время проникновения с толщиной при различных температурах, приводятся в публикациях ASTM, посвященных методам испытаний. В таблице 3.4 приводятся данные, которые могут быть использованы, чтобы рассчитать толщину, исходя из времени проникновения при испытаниях.
Таблица 3.4 - Время необходимое
для растворения 25 мкм цинка
|
Температура испытания °С |
Время, сек. |
|
15,6 21,1 26,7 32,2 37,8 |
115 105 93 88 80 |
При этом методе не нужно прерывать испытания, чтобы определить момент его окончания. Главный недостаток этого метода состоит в том, что испытания необходимо проводить при определённой температуре, что не всегда возможно. Реактивы должны использоваться только однократно.
Контроль по внешнему виду. Детали, покрытые цинком, осматриваются невооружённым глазом при освещении рассеянным светом. Отбраковке подлежат детали, имеющие следующие дефекты покрытия: непокрытые участки поверхности, шероховатость, превышающая допустимые нормы, отслаивание покрытия в виде отдельных вздутий (пузырей) или осыпающихся частиц покрытия, точечные изъязвления (питтинг), грязные подтёки воды, тёмно-коричневый цвет пассивной плёнки.
Допустимые дефекты покрытий перечислены в разделе 3.1.
Контроль прочности сцепления. Для оценки прочности сцепления применяют испытание нанесением сетки царапин. На поверхность испытуемого покрытия наносят стальным остриём несколько параллельных линий до основного металла на расстоянии 2‑3 мм друг от друга и параллельных линий, проведённых перпендикулярно к первым линиям. Покрытие считается выдержавшим испытание, если образовавшиеся в пересечении квадратики не отслаиваются при растирании пальцем.
3.8.4 Дефекты и их устранение
Цинковое покрытие с поверхности стальных деталей может быть удалено растворением в 5–10 % соляной кислоте или серной кислоте при комнатной температуре. Чтобы уменьшить степень растворения стали, в раствор добавляют немного окиси сурьмы или хлорида сурьмы (3–5 г/л). Для растворения цинка можно использовать 10–15 % раствор щёлочи.
Основные неполадки при цинковании и способы их устранения приведены в таблице 3.5.
Таблица 3.5 – Неполадки при цинковании в цинкатном электролите
|
Характеристика дефектов |
Причины дефектов |
Способы устранения |
|
Тёмный (губчатый) осадок |
1)наличие олова в двухвалентной форме 2)низкое содержание олова 3)низкая концентрация ZnO 4)повышенная катодная плотность тока 5)низкая температура электролита 6)электролит не проработан |
1) провести корректировку электролита по соответствующим компонентам 2) повысить температуру 3) снизить плотность тока 4) проработать электролит |
|
Отсутствие покрытия по всей поверхности изделия при низких плотностях тока |
1)короткое замыкание на ванне 2)наличие окислителей в электролите |
1) устранить короткое замыкание 2) произвести проработку ванны током |
|
Пассивирование анодов, сопровождаемое выделением кислорода |
1)недостаток щёлочи 2)высокое значение анодной плотности тока |
1) увеличить поверхность анодов 2) снизить плотность тока |
Характерные неполадки при пассивировании представлены в таблице 3.6.
Таблица 3.6 – Неполадки при пассивировании
|
Характеристика неполадок |
Причина неполадок |
Способ устранения |
|
Образование коричневой легко стирающейся плёнки |
Увеличение рН раствора; передержка деталей в растворе |
Добавить серную кислоту до заданного рН; сократить время выдержки |
|
Пятна на внутренних поверхностях деталей |
Разбавление в растворе |
Добавить свежий раствор в концентрированном виде |
|
Плёнка синеватого цвета |
Недостаток бихроматов |
Добавить соль Ликонда25 |
|
Наличие участков, не покрытых плёнкой |
Некачественная промывка перед пассивированием |
Улучшить промывку |
3.8.5 Анализ электролитов
Анализ растворов для обезжиривания. В растворах для обезжиривания проводится обработка стальных деталей. Основными компонентами ванн являются: едкий натр, тринатрийфосфат и силикат натрия.
1) Определение едкого натра проводится объёмным методом. Гидроксид бария Ba(OH)2 титруют раствором соляной кислоты в присутствии индикатора фенолфталеина. Фосфат натрия и силикат натрия при действии хлорида бария переходят в осадок. Реакция осаждения протекает по уравнениям
2 Na3PO4 + 3 BaCl2 ® Ba3(PO4)2 + 6 NaCl, (3.7)
Na2SiO3 + BaCl2 ® BaSiO3 + 2 NaCl. (3.8)
Едкий натр даёт эквивалентное количество гидроксида бария
2 NaOH + BaCl2 ® Ba(OH)2 + 2 NaCl. (3.9)
Реакция титрования идёт по уравнению
Ba(OH)2 + 2 HCl ® BaCl2 + 2 H2O. (3.10)
Ход анализа подробно описан в [9].
2) Определение общей щёлочности раствора. При большом содержании едкого натра и карбонатов в присутствии тринатрийфосфата и жидкого стекла раздельное определение едкой щёлочи и карбонатов не даёт удовлетворительных результатов. Поэтому в обезжиривающем растворе определяют общее содержание щёлочи в пересчёте на едкий натр титрованием раствора соляной кислоты в присутствии метилового оранжевого. Ход анализа подробно описан в [9].
3) Определение тринатрийфосфата проводится фотоколориметрическим методом. Метод основан на восстановлении молибдена, входящего в состав фосфорно-молибденовой гетерополикислоты Н7[P(Mo2O7)6], до пятивалентного при помощи двухвалентного железа и сульфита натрия. Раствор окрашивается в синий цвет (молибденовой сини). Измерение интенсивности окраски проводят на приборе ФЭК–2 с зелёным светофильтром в кювете с толщиной слоя 20–30 мм в зависимости от содержания тринатрийфосфата. Ход анализа подробно описан в [9].
4) Определение содержания силиката натрия. Содержание силиката натрия в растворе вычисляют после определения кремния. Кремний в растворе определяют фотоколориметрическим методом. Соли кремния образуют с молибдатом аммония в слабокислом растворе жёлтое комплексное соединение кремнемолибденовой кислоты. При последующем восстановлении кремнемолибденовой кислоты с помощью хлорида олова молибден восстанавливается до низшей степени окисления с образованием молибденовой сини. Измерение интенсивности окраски проводят на приборе ФЭК–2 с зелёным светофильтром в кювете с толщиной слоя 20–30 мм в зависимости от содержания силиката натрия в растворе. Ход анализа подробно описан в [9].
Анализ раствора травления. В растворе травления анализируются содержание серной кислоты и содержание примеси железа.
1) Определение серной кислоты производится ацидиметрическим методом. Метод основан на определении общей кислотности раствора титрованием пробы щёлочью по фенолфталеину. Ход анализа подробно описан в [8].
2) Определение железа производится комплексонометрическим методом. Метод основан на прямом титровании трилоном Б железа (III) в присутствии салициловой кислоты при рН 4–5. Предварительно двухвалентное железо окисляют до трёхвалентного перекисью водорода. Ход анализа подробно описан в [8].
Анализ цинкатного электролита цинкования.
1)II) до (III). Определение железа заканчивают весовым методом. Методика проведения анализа подробно изложена в [8].
2)
3)
3.8.6 Обслуживание электролитов
В процессе работы ванны цинковые аноды покрываются шламом, присутствие которого затрудняет их растворение, что приводит к постепенному истощению электролита цинком. Для удаления шлама с анодов нужно периодически извлекать их из ванны и чистить железными щётками.
Для очистки электролита цинкования от примесей металлов (железо, медь, свинец и др.), источниками которых могут быть используемые технические химические продукты или медные детали ванн, применяют методы селективной электролитической обработки электролитов при плотности тока 20–30 А/м2.
Железо удаляют путём окисления Fe2+ в Fe3+ введением в нагретый до 70–80°С электролит перекиси водорода (0,5 мл/л) и осаждения Fe3+ в виде гидроокиси воздействием щелочных реагентов.
Для очистки электролита от органических примесей рекомендуется профильтровать электролит через активированный уголь. Для очистки электролита от загрязнения желатином, клеем и другими органическими веществами добавляют раствор танина из расчёта 0,1 г/л, а образующийся осадок отфильтровывают.
Очистка от примесей ионов меди, кадмия и других металлов эффективна с помощью цинковой пыли или гранул, размеров от 1 до 5 мм. Электролит подаётся в аппарат под давлением для создания псевдоожиженного слоя части цинка. Благодаря высокой скорости подачи раствора и турбулизации движения обеспечивается непрерывное контактирование между гранулами, быстрое отслаивание и удаление медно-кадмиевого слоя с поверхности гранул, а очищенная поверхность снова активно вступает в реакцию с соединениями примесных металлов. Скорость пропускания электролита через слой цинковых гранул 0,03–0,5 м/с; температура 40–50°С. Электролит анализируют и корректируют не реже двух раз в месяц.
3.9 Утилизация цинка из промывных вод и очистка сточных вод
В данном курсовом проекте предусмотрен процесс утилизации цинка из промывных вод ванны улавливания. Схема этого процесса изображена на рисунке 3.2.

Рисунок 3.2 – Схема утилизации цинка из промывных вод
Принцип работы схемы следующий: детали из ванны покрытия поступают в ванну улавливания. В этой ванне при отмывкецинка образуется нерастворимый гидрооксид цинка (Zn(OH)2) в виде белой мути. Так как расход воды на промывку невелик, то вся промывная вода подаётся в отстойник. В отстойнике Zn(OH)2 оседает на дне, а разбавленный NaOH над осадком подаётся на очистные сооружения. По мере того как в отстойнике скапливается гидрооксид цинка, периодически в отстойник сливается щелочь из ванны цинкования. В отстойнике гидроксид цинка растворяется, так как концентрация скачиваемой щёлочи большая, а затем полученный раствор через фильтр перекачивается обратно в ванну покрытия. На фильтре раствор очищается от гидроксида железа и других нерастворившихся примесей.

1)серная кислота; 2)бисульфит натрия; 3)известь; 4)хромсодержащие стоки; 5)кислые стоки; 6)щелочные стоки; 7)стоки, содержащие ионы тяжёлых металлов; 8)очистка от хроматов; 9)нейтрализация; 10)вакуум-фильтр; 11)отстойник.
Рисунок 3.3 – Общая схема канализирования и очистки сточных вод цехов гальванических покрытий
Промывные воды со всех остальныхванн собираются и подвергаются очистке реагентным способом. Этот метод основан на реакциях нейтрализации и окисления-восстановления. Достоинствами его являются: простота оборудования и его эксплуатации, универсальность, дешевизна реагентов. Недостатки метода: необходимость в больших площадях для установки громоздкого оборудования; большой расход реагентов; проблемы с обезводораживанием и захоронением шламов; невозможность использования воды в обороте; невозможность извлечения ценных металлов.
Общая схема канализирования и очистки сточных вод цеха гальванического покрытия приведена на рисунке 3.3.
Обезвреживание хромсодержащих сточных вод. Обезвреживание хрома ведётся раствором бисульфита натрия (NaHSO4) при рН 2–2,5 по реакции:
2 CrO3 + 6 NaHSO4 + 3 H2SO4 Þ 3 Na2SO4 + 2 Cr2(SO4)3 + 6 H2O. (3.11)
При дальнейшем попадании в ванну для обезвреживания кислых и щелочных сточных вод происходит следующая реакция:
2 Cr2(SO4)3 + 12 NaOH Þ 4 Cr(OH)3¯+ 6 Na2SO4. (3.12)
Гидроокись хрома выпадает в виде шлама.
Обезвреживание кислых и щелочных вод. В ванну для обезвреживания кислых и щелочных стоков поступают сточные воды из ванны обезвреживания хромовых соединений с рН 2–2,5; кроме того, в эту же ванну поступают воды непосредственно от промывных ванн, стоящих после травления, активации и обезжиривания. Происходит взаимная частичная нейтрализация. Если при этом в растворе преобладает кислота, то в ванну поступает щёлочь, если щёлочь, то в ванну поступает кислота. Рекомендуемое рН сточных вод, уходящих в заводскую канализацию, 7,5–8,5. Обезвреженные воды поступают в промежуточную насосную ёмкость, из неё по мере наполнения выкачиваются насосами в отстойник, а оттуда самотёком – в заводскую канализацию.
Очистка сточных вод от органических загрязнений. В промывные воды попадают смазочно-охлаждающие жидкости (СОЖ), которые удаляются с деталей в ваннах обезжиривания. Кроме того, из ванны пассивирования в промывные воды попадает поливиниловый спирт. Смазочно-охлаждающие жидкости представляют собой жиры, эти жиры частично задерживаются на шламе, который образуется при реагентной очистке. Далее этот шлам отправляется в отвал. После реагентной очистки сточные воды пропускаются через ёмкости с активированным углём, где органические примеси адсорбируются на поверхности активного угля.
Помещение, в котором находится установка обезвреживания сточных вод, должно быть оборудовано вытяжной вентиляцией.
4 РАСЧЁТНАЯ ЧАСТЬ
4.1 Выбор основного типа оборудования
Главный исполнительный механизм автооператорной линии – это автооператор. В настоящее время широко распространены три типа автооператоров: подвесной, портальный и консольный. В данном курсовом проекте используется портальный автооператор, так как он прост в изготовлении и достаточно грузоподъёмен. Используя справочные данные [23], выбираем автооператор портального типа Г007 со следующими характеристиками:
1) кг;
2) мм;
3) м/с;
4) м/с;
5) мм;
6) кг.
Так как покрытие наносится на довольно мелкие детали, то их целесообразнее обрабатывать в барабанах насыпью. Используя справочные данные [23], выбираем барабан типа НПК–3МК со следующими характеристиками:
1) кг;
2) об/мин;
3) мм;
4) мм;
5) мм;
6) кг.
Процесс цинкования ведётся на автоматической гальванической линии производительностью 32 м2/ч (320 кг/ч) и единовременной загрузкой в барабан 2,5 м2 (25 кг) [23]. В данной автоматической гальванической линии используются ванны следующих габаритных размеров [23]:
1) мм;
2) мм.
4.2 Конструктивный расчёт основного оборудования
Поскольку на автооператорной линии детали обрабатываются в барабанах, то объём барабана шестигранной формы определяется по формуле:
Vб= 2,6 × r2б × Lб, (4.1)
где rб – радиус описанной окружности барабана, м;
Lб – длинна барабана, м.
Vб= 2,6 × 0,1702 × 0,610= 0,0458 м2.
Общее время нанесения покрытия в ванне составит:
t= t’т + tоб, (4.2)
где t’т – технологическое время, с;
tоб – время обслуживания, необходимое для загрузки деталей в ванну и выгрузки их из ванны, с (принимаем tоб=60 с).
 (4.3)
(4.3)
где d - средняя толщина наносимого покрытия, дм;
r - плотность металла покрытия, кг/дм3;
i - средняя катодная плотность тока, А/дм2;
кэ – электрохимический эквивалент металла покрытия, кг/А·ч;
ВТ – выход по току металла покрытия, ед.
 с.
с.
Так как процесс покрытия идёт в барабанах при активном перемешивании, то часть покрытого металла истирается, чтобы это учесть увеличим tт на 30%:
t’т= 1660 × 1,3= 2158 с.
t= 2158 + 60= 2218 с.
Далее определим ритм автооператорной линии по формуле:
 (4.4)
(4.4)
где Т0 – действительный годовой фонд времени работы оборудования (для двухсменной работы Т0=3810 ч);
h - коэффициент, показывающий какую долю рабочего дня АОЛ выдаёт барабаны с покрытыми деталями (принимаем h=0,85);
nЕ3 – годовая программа в единичных загрузках:
nЕ3= Sгод / Sез, (4.5)
где Sез – площадь единичной загрузки, м2;
Sгод – величина, связанная с производственной программой S соотношением:
Sгод= S× (1 + 0,01 × a), (4.6)
где a - процент исправимого брака при нанесении покрытий (принимаем a=5).
Sгод= 50000 × (1 + 0,01 × 5)= 52500 м2.
nЕ3= 52500 / 2,5= 21000 загр/год.
 с.
с.
Количество основных ванн для нанесения покрытия определяем по формуле:
nов = t / Rр, (4.7)
nов = 2218 / 555= 3,99 » 4
Аналогично рассчитываем количество ванн для остальных процессов. В результате расчёта получаем четыре ванны цинкования, две сушильных камеры, остальных ванн по одной.
Определяем время цикла работы автооператорной линии:
tц= К × Rр, (4.8)
где К – наименьшее общее кратное для принятых количеств ванн (К=4).
tц= 4 × 555= 2220 с (37 мин.).
Необходимое количество автооператоров:
nа = tа / Rр, (4.9)
где tа – суммарное время обслуживания автооператорами всех ванн.
Величина tа складывается из суммарного времени горизонтальных перемещений tг, вертикальных перемещений tв и выстоя tвыст автооператоров над всеми ваннами:
tа= tг + tв + tвыст. (4.10)
 (4.11)
(4.11)
где Wср– среднее расстояние между осями соседних ванн (Wср =1,5 м);
nпоз – количество позиций в линии, обслуживаемых автооператором за один ритм (nпоз =16);
Vг – скорость горизонтального перемещения автооператора (Vг =0,2 м/с);
К – коэффициент, учитывающий холостые ходы оператора и компоновку ванн (К= 4).
 с.
с.
Суммарное время вертикальных перемещений:
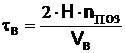 (4.12)
(4.12)
где Н – высота подъёма каретки автооператора (Н= 1,3 м);
Vв – скорость вертикального перемещения автооператора (Vв =0,11 м/с).
 с.
с.
Суммарное время выстоя над ваннамиtвыст равно 543 сек.[13]
tа= 450 + 378 + 543= 1371 с.
nа = 1371 / 555= 2,47 » 3
Необходимое количество автооператоров равно трём.
Далее рассчитаем наиболее существенный габаритный размер автооператорной линии - длину. Её находим по формуле:
L= n×W + nс×Wc + W3/P + DWC + n0×DW0 + n1×DW1 + n2×DW2 + Wб, (4.13)
где n – количество ванн одного типоразмера;
W – ширина ванн принятого типоразмера;
nс – количество сушильных камер;
Wc – ширина сушильной камеры;
W3/P – ширина загрузо-разгрузочной стойки;
DWC – зазор между сушильной камерой и загрузо-разгрузочной стойкой;
n0 – количество комбинаций соседних ванн без бортовых отсосов;
DW0 - зазор между ваннами без бортовых отсосов;
n1 – количество односторонних бортовых отсосов;
DW1 - зазор между стенками ванн с односторонним бортовым отсосом;
n2 – количество двухсторонних бортовых отсосов;
DW2 - зазор между стенками ванн с двухсторонним бортовым отсосом;
Wб – ширина одностороннего бортового отсоса по краю линии.
L= (12×0,63+5·0,8)+2×0,8+0,6+0,3+10×0,16+3×0,29+3×0,39+0= 17,7 м.
На основании рассчитанных данных построена циклограмма, которая изображена на рисунке 4.1.



Рисунок 4.1 – Циклограмма автооператорной линии цинкования в барабанах.
Условные обозначения: З – загрузка, С – сушка, ПТ – тёплая промывка после хроматирования, ПХ – промывка холодная после хроматирования, Х – хроматирование, О – химическое обезжиривание, ПТо – тёплая промывка после обезжиривания, Оэ – электрохимическое обезжиривание, ПТэ - тёплая промывка после электрохимического обезжиривания, А – активация, ПХУ – промывка холодная после цинкования, УЦ – улавливание после цинкования, ПХа – холодная промывка после активации, Ц – цинкование, ▲ – подъём барабана автооператором и выстой для стекания раствора (16 с.), ▼ – опускание барабана автооператором (10 с.), ¤ – перемещение автооператора на одну позицию (8 с.), ▬ – ванна с барабаном.
Время каждой операции согласно циклограмме отражено в итоговой таблице 4.1.
Таблица 4.1 – Продолжительность технологических операций
|
Наименование операции |
Время по технологии, с. |
Время по циклограмме, с. |
|
Загрузка Обезжиривание Промывка после обезжиривания Электрохимическое обезжиривание Промывка после электрохим. обезжиривания Активация Промывка после активации: первая ступень втораяступень Цинкование Улавливание после цинкования Промывка после цинкования Хроматирование Промывка после хроматирования: первая ступень втораяступень Сушка |
– 120-300 ≥20 30-300 ≥20 ≥20 15-45 30-150 1200-5400 ≥20 ≥20 45-90 ≥20 ≥20 180-600 |
407 164 84 28 28 31 56 20 20 1944 128 20 56 60 195 1010 |
4.3 Электрический расчёт электрохимических ванн
Сила тока I на ванне определяется произведением технологической плотности тока iср и площади единичной загрузки Sез:
I = 1,05 × iср× Sез, (4.14)
Коэффициент 1,05 учитывает потери электричества на контакты деталей в барабане.
Напряжение на ванне при покрытии деталей в барабанах определяется по формуле:
U= (1 - b) × [Ea – Ek + (1 + a) × I × R + DUП], (4.15)
где DUП – падение напряжения в перфорации барабана, В;
b - коэффициент, учитывающий потери напряжения в контактах;
a - коэффициент, учитывающий увеличение падения напряжения за счёт газонаполнения;
R – сопротивление электролита;
Ea,Ek – потенциалы катода и анода при верхних плотностях тока,В.
Падение напряжения в электролите I×R определяют по формуле:
 (4.16)
(4.16)
где c - электропроводность электролита;
icp – средняя плотность тока, определяемая по формуле:
 (4.17)
(4.17)
где iк,iа – катодная и анодная плотности тока;
Lср – среднее расстояние до деталей, определяется по формуле:
Lср = (Lд + Lб) / 2, (4.18)
где Lб – расстояние от анода до ближних деталей в барабане;
Lд - расстояние от анода до центра барабана.
Lд = Wшт / 2, (4.19)
Lб = (Wшт / 2) - rбар, (4.20)
где Wшт – расстояние между анодными штангами;
rбар – радиус описанной окружности барабана.
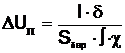 (4.21)
(4.21)
где d - толщина стенки барабана;
ò - степень перфорации барабана.
Боковая перфорированная поверхность барабана, прогруженная в электролит:
Sбар = 6 ×Lбар ×Wгр × 2/3, (4.22)
где Lбар – длинна барабана;
Wгр – ширина грани барабана.
Ванна цинкования:
Lбар=0,61 м; Wгр=0,17 м; ò=0,2; d=0,01 м; a=0,01; b=0,02; c=30 Ом-1×м-1;Sез=2,5 м2; Ea=–1,39 В; Ek=–1,6 В; Wшт=0,6 м; rбар=0,17 м; iк=100 А/м2; iа=150 А/м2.
Sбар = 6 × 0,61 × 0,17× 2/3 = 0,4148 м2,
 А/м2,
А/м2,
Lд = 0,6 / 2 = 0,3 м,
Lб = (0,6 / 2) – 0,17 = 0,13 м,
Lср = (0,3 + 0,13) / 2 = 0,215 м,
I = 1,05 × 122,47 × 2,5 = 321,5 А,
 В,
В,
 В,
В,
U= (1 – 0,02) × [–1,39 + 1,6 + (1 + 0,01) × 0,88 + 1,29] = 2,34 В.
Ванна электрохимического обезжиривания:
Lбар=0,61 м; Wгр=0,17 м; ò=0,2; d=0,01 м; a=0,2; b=0,02; c=40 Ом-1×м-1;Sез=2,5 м2; Ea=–1,58 В; Ek=–0,9 В; Wшт=0,6 м; rбар=0,17 м; iк=500 А/м2; iа=150 А/м2.
Sбар = 6 × 0,61 × 0,17× 2/3 = 0,4148 м2,
 А/м2,
А/м2,
Lд = 0,6 / 2 = 0,3 м,
Lб = (0,6 / 2) – 0,17 = 0,13 м,
Lср = (0,3 + 0,13) / 2 = 0,215 м,
I = 1,05 × 273,86 × 2,5 = 718,88 А,
 В,
В,
 В,
В,
U= (1 – 0,02) × [–1,58 + 0,9 + (1 + 0,2) × 1,47 + 2,16] = 3,18 В.
На основании проведённых расчётов подбираем источники постоянного тока [23]:
1)
2)
4.4 Тепловой расчёт
4.4.1. Тепловой расчет нагревающихся ванн
Определение расхода теплоты на разогрев ванны. Количество теплоты Qраз необходимое для разогрева ванны, складывается из расхода Q1 на разогрев раствора,материала и футеровки ванны и расхода Q2 на компенсацию тепловыхпотерьв окружающую среду:
Qраз = Q1 + Q2 / 2, (4.23)
где Q2 - тепловые потери при рабочей температуре за время разогрева ванны; принимается,что в процессе разогрева тепловые потери в 2 раза ниже. ВеличинуQ1 определяют как:
Q1 = (V1×c1×r1 + c2×m2 + c3×m3) ×(tK – tH), (4.24)
гдеV1,c1,r1 - соответственно объем, удельная массовая теплоемкость и плотность нагреваемого раствора;
с1 и с2 – теплоемкость материалов корпуса ванны и футеровки (для стали - 500 Дж/(кг·К); для пластиката - 1630 Дж/(кг·К));
m2 и m3 - массы корпуса ванны и футеровки;
tк и tн - конечная и начальная температуры раствора.
Для разбавленных растворов (с общей концентрацией компонентов до 100 кг/м3) допустимо для ориентировочных расчетов принять плотность и теплоемкость воды 1000 кг/м3 и 4180 Дж/(кг·К).
Q3, а также иQ4 определяем приближенно путем перемножения величины теплоотдающей поверхности (корпуса ванны FK или зеркала электролита Fз) на величину удельных потерь теплоты q через стенки ванны или через зеркало электролита и на время разогрева ванны tр:
Q3 = q3·FK·tр , (4.25)
Q4 = q4·F3·tр . (4.26)
Величина удельных потерь теплоты qз (Вт/м2) через стенки ванны в интервале температурt в ванне 40-100°С равна :
q3 = b0 + b1·t (4.27)
b0 , b1 – коэффициенты по [13, табл. 4.2].
Удельные теплопотери q4 (Вт/м2) через зеркало электролита в интервале его температуры t=30-100°С могут быть вычислены по эмпирическому уравнению:
q4 = 82 + 0,0115·t3. (4.28)
Ванна электрохимического обезжиривания:
Ср-ра≈ 4180 Дж/кг·К, rр-ра≈ 1000 кг/м3, габариты ванны 1,25×0,8×1 м, rф= 1,5 кг/см3, rм.в.= 7,8 кг/см3, d= 0,04 дм, tр= 7200 с.
V1 = 1,25·0,8·(1 – 0,2)= 0,8 м3 = 800 л,
Sдна= 1,25·0,8 = 1 м2 = 100 дм2,
Sбок= 1,25·1·0,2 + 0,8·1·0,2= 4,1 м2 = 410 дм2,
Sванны = 100 + 410 = 510 дм2,
Vм.в.= 510·0,04= 20,4 дм3, Vм.ф.= 510·0,04= 20,4 дм3,
mм.в.= 20,4·7,8= 159,12 кг (сталь 3),
mф= 20,4·1,5= 30,6 кг (пластикат),
Q1=(800·4180·1+500·159,12+1630·30,6)·(60–20)=138937,5 кДж,
q3= -183,124 + 7,553·60 = 270 Вт/м2,
Q3= 270·5,1·7200= 9916,4 кДж,
q4= 82 + 0,0115·603 = 2566 Вт/м2,
Q4= 2566·1·7200= 18475,2 кДж,
Q2= 9916,4 + 18475,2 = 28391,6 кДж,
Qраз= 138937,5 + 28391,6 / 2 = 153133,3 кДж.
Определение расхода теплоты на поддержание рабочей температуры. Количество теплоты Qраб необходимое для поддержания рабочей температуры в ванне химической обработки, складывается из расхода теплоты Q2 на компенсацию тепловых потерь в окружающую среду и расхода теплотыQ5 на нагрев приспособлений с деталями, периодически поступающих в ванну. Для ванн электрохимической обработки из суммы Q2 иQ5 следует вычесть величину Q6 - количество теплоты, выделяющейся при прохождении через ванну электрического тока. Таким образом,
Qраб= Q2 + Q5 – Q6 , (4.29)
Расчет величины Qраб удобно вести на 1 час. В этом случае величины Q2, Q5и Q6 могут быть вычислены по уравнениям:
Q2 =3600·(q3 ·Fк + q4 ·Fз), (4.30)
Q5= (с4×m4 + c5×m5) ×(tK – tH)·nезчас, (4.31)
Q6= I·(U–Eтепл)·tтчас, (4.32)
где с4 и с5 - удельные теплоемкости материалов барабана (винипласт 1630 Дж/(кг·К)) и обрабатываемых деталей (сталь 500 Дж/(кг·К));
m4 и m5 – массы барабана (10 кг) и обрабатываемых деталей одной единичной загрузки (25 кг);
nезчас – количество загрузочных единиц, обрабатываемых в ванне за 1 час (определяем по циклограмме);
Етепл – тепловое напряжение разложения;
tтчас – суммарное технологическое время обработки деталей в ванне в течение часа (определяем по циклограмме).
Тепловое напряжение разложения для взаимообратимых электрохимических процессов (осаждение металла с растворимым анодом) равно 0; для прочих процессов величину Етепл можно вычислить из выражения:
Етепл ,
(4.33)
,
(4.33)
где DН - изменение энтальпии в электрохимическом процессе;
z – число электронов, участвующих в реакции;
F – число Фарадея.
Ванна электрохимического обезжиривания:
Q5= (1630·10 + 500·25)·(60–20)·6= 6912 кДж,
Q2= 21071,3 кДж (см. выше),
H2O®H2 + ½ O2,
DH= DHобводы – DHобводор. – DHобкисл.,
DH= - 285,58 –0 –0 = - 285,58 кДж/моль,
Етепл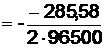 = 1,48 В,
= 1,48 В,
tтчас= 28/(28 +527)= 0,05 ч= 182 с,
Q6= 718,88·(3,18 – 1,48)·182= 222 кДж,
Qраб= 21071,3 + 6912 – 222= 27 761,3 кДж.
4.4.2 Расчёт змеевика.
Поверхность змеевика Sзм равна:
 (4.34)
(4.34)
где к –теплопередачи от конденсирующегося пара к нагреваемому водному раствору;
Dtср - средний температурный напор;
tр - время разогрева ванны (7200 с).
Коэффициент к зависит от характера движения жидкости в ванне, толщины трубы змеевика, наличия на ней продуктов коррозии и загрязнений. В случае свободного движения электролита к=1000 Вт/м2·ч.
Средний температурный напор вычисляют как:
 , (4.35)
, (4.35)
где tпн и tн - соответственно начальные температуры пара (130°С) и нагреваемого раствора (20°С):
tкк и tк - конечные температуры конденсата (110°С) и раствора (60°С).
После расчета теплоотдающей поверхности змеевика Sзм можно рассчитать его длину Lзм, предварительно задавшись наружным диаметром трубы d=21·10-3 м.
Lзм= Sзм/(p· d), (4.36)
Расход пара в период разогрева составит:
mпраз= Qраз/(Iп – Iконд), (4.37)
гдеIп и Iконд - соответственно удельное теплосодержание (энтальпия) греющего пара и конденсата (Iп =2726 кДж/кг;Iконд =546,8 кДж/кг). Аналогично часовой расход пара на поддержание рабочей температуры будет равен:
mпраб= Qраб/(Iп – Iконд),(4.38)
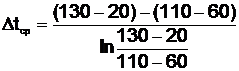 °С,
°С,
 м2,
м2,
Lзм= 0,273/(3,14· 21·10-3)= 4,14 м,
mпраз= 149473,2/(2726 – 546,8)= 68,6 кг/час,
mпраб= 27761,3/(2726 – 546,8)= 12,7 кг/час.
4.4.3 Укрупнённый тепловой расчёт ванн
При расчётах учитываем, что в году по скользящему графику 8 праздничных дней, 97 выходных дней и 260 рабочих.
Расход пара на разогрев:
mпчас=24·(tк – tн), (4.39)
Для ванны обезжиривания:
mпчас = 2,4·(60-20)= 96 кг/час.
Расход пара на поддержание температуры mрабчас определяется по таблице 4.3 [13].
Для ванны обезжиривания mрабчас=10 кг/час.
Результаты укрупнённого расчёта отображены в таблице 4.2.
Таблица 4.2 – Укрупнённый тепловой расчёт ванн
|
Наименование ванны |
Количество ванн |
tк,°С |
mпчас, кг/час |
mпгод, кг/год |
mрабчас, кг/час |
mрабгод, кг/год |
|
Обезжиривание |
1 |
60 |
60,48 |
15724,8 |
9,765 |
38083,5 |
|
Промывка тёплая |
3 |
50 |
45,36 |
11793,6 |
50,4 |
196560 |
|
Сумма |
196,56 |
51105,6 |
160,965 |
627763,5 |
4.5 Материальные расчёты
4.5.1 Расчёт расхода воды на промывку
Расчёт расхода воды на промывку производится в соответствии с ГОСТ 9.305-84. Согласно этому ГОСТу при погружном способе промывки, независимо от её схемы, расход воды определяется по формуле:
 (4.40)
(4.40)
где q – удельный вынос электролита (раствора) из ванны поверхностью деталей в барабане (q= 0,4 дм3/м2);
N – количество ступеней (ванн) промывки;
k0 – критерий окончательной промывки деталей;
F – промываемая поверхность деталей (F= 16,2 м2/ч).
k0= С0 / Сп, (4.41)
где С0 – концентрация основного компонента в электролите в ванне перед промывкой, г/л;
Сп – допустимая концентрация основного компонента в электролите после промывки, г/л.
Пример расчёта расхода воды на операцию химическое обезжиривание:
С0=46,25 г/л; Сп=0,8 г/л; q= 0,4 дм3/м2; F= 16,2 м2/ч; N=1
k0= 46,25 / 0,8 = 57,81; Q= 0,4×16,2×57,81 = 374,2 л/ч
Результаты расчёта расхода воды на промывку сведены в таблице 4.3.
Таблица 4.3 – Расходы воды на промывку.
|
Операция перед промывкой |
Схема промывки |
С0, г/л |
Сп, г/л |
К0 |
Qуд, л/м2 |
Q, л/ч |
|
Химическое обезжиривание |
|
46,25 |
0,8 |
57,8 |
23,1 |
374,2 |
|
Электрохимическое обезжиривание |
|
46,25 |
0,1 |
462,5 |
8,6 |
139,3 |
|
Активация |
|
100,7 |
0,05 |
2014 |
17,9 |
289,9 |
|
Цинкование |
|
13,5 |
0,01 |
1350 |
14,7 |
238,1 |
|
Пассивирование |
|
72,5 |
0,01 |
7250 |
23,8 |
386,2 |
|
Сумма |
88,1 |
1427,7 |
4.5.2 Расчёт расхода химикатов и анодов
Расчёт расхода химикатов на первоначальное приготовление рабочего раствора рассчитывается по формуле:
mi= Ci × Vi × nB × nCM, (4.42)
где mi – масса каждого компонента раствора, кг;
Ci – концентрация каждого компонента раствора, г/л;
Vi – объём ванны (для электрохимических ванн V=800 л, для химических ванн V=630 л);
nB – количество ванн;
nCM – сменность ванны в год (ванна цинкования 1 раз, ванна пассивации 6 раз, остальные 12 раз).
Пример расчёта для ванны обезжиривания:
 = 30 ×
0,63 ×
1 ×
12 = 226,8 кг;
= 30 ×
0,63 ×
1 ×
12 = 226,8 кг;  = 10 ×
0,63 ×
1 ×
12 = 75,6 кг;
= 10 ×
0,63 ×
1 ×
12 = 75,6 кг;  = 20 ×
0,63 ×
1 ×
12 = 151,2 кг; mдв-301=
4 ×
0,63 ×
1 ×
12 = 30,3 кг.
= 20 ×
0,63 ×
1 ×
12 = 151,2 кг; mдв-301=
4 ×
0,63 ×
1 ×
12 = 30,3 кг.
Результаты расчётов приведены в таблице 4.4.
Таблица 4.4 – Расход химикатов на приготовление растворов.
|
Наименование ванны |
Состав раствора |
Концентрация, г/л |
Масса, кг |
|
Химическое обезжиривание |
NaOH Na3PO4 Na2SiO3 ДВ-301 |
30 10 20 4 |
226,8 75,6 151,2 30,3 |
|
Электрохимическое обезжиривание |
NaOH Na3PO4 Na2SiO3 ДВ-301 |
30 10 20 1,45 |
288 96 192 14 |
|
Активация |
HCl |
75 |
567 |
|
Цинкование |
ZnO NaOH НБЦ-О НБЦ-К |
13,5 105 5 5 |
10,9 84 4 4 |
|
Пассивация |
Соль Ликонда-25 Спирт поливиниловый |
72,5 4 |
274 15 |
Расчёт химикатов на корректировку проводится по формуле:
miкор = [(qунос + qв + qф ) ×Ci + qразл ] ×Sгод, (4.43)
где qунос – потери раствора с деталями и барабаном (qунос=0,4 дм3/м2);
qв – потери раствора в вентиляцию (qв=0,015 дм3/м2);
qф – потери раствора при фильтрации (только в ванне цинкования qф=0,065 дм3/м2);
Ci – концентрация компонента, г/л;
qразл – потери химикатов при разложении их электрическим током (только у электрохимических ванн qразл=0,25 дм3/м2 [6]);
Sгод – годовая производственная программа, м2/год.
Пример расчёта для обезжиривания:
 ×30 + 0] ×52,500 = 653,6 кг;
×30 + 0] ×52,500 = 653,6 кг;  ×10 + 0] ×52,500 = 217,9 кг;
×10 + 0] ×52,500 = 217,9 кг;  ×20 + 0] ×52,500 = 435,8 кг;
×20 + 0] ×52,500 = 435,8 кг;  ×4 + 0] ×52,500
= 87,2 кг.
×4 + 0] ×52,500
= 87,2 кг.
Результаты расчета приведены в таблице 4.5.
Таблица 4.5 – Расход химикатов на корректировку растворов.
|
Наименование ванны |
Состав раствора |
Концентрация, г/л |
Масса, кг |
|
Химическое обезжиривание |
NaOH Na3PO4 Na2SiO3 ДВ-301 |
30 10 20 4 |
653,6 217,9 435,8 87,2 |
|
Электрохимическое обезжиривание |
NaOH Na3PO4 Na2SiO3 ДВ-301 |
30 10 20 1,45 |
666,8 231 448,9 44,7 |
|
Активация |
HCl |
75 |
1634 |
|
Цинкование |
ZnO NaOH НБЦ-О НБЦ-К |
13,5 105 5 5 |
– 2659,2 139,2 139,2 |
|
Пассивация |
Соль Ликонда-25 Спирт поливиниловый |
72,5 4 |
1579,6 87,2 |
Расчёт анодов на первоначальный пуск рассчитывается по формуле:
Sанобщ = I / iа, (4.44)
где I – сила тока, А;
iа – анодная плотность тока, А/м2.
Sанобщ = 321,5 / 150 = 2,15 м2.
Массу одного анода берём равную 15 кг, плотность цинка r=7200 кг/м3, отсюда находим объём одного анода:
V= 15 / 7200 = 0,0021 м3.
Vаобщ = Sанобщ × dZn1, (4.45)
где dZn1 – толщина одного анода, м.
Vаобщ = 2,15 × 0,012 = 0,0258 м3.
Общее число анодов определяем по формуле:
Па = Vаобщ / V, (4.46)
Па = 0,0258 / 0,0021 = 12,28 » 13.
На выполнение годовой программы:
mагод = Sгод × d × r × к1 × к2, (4.47)
где d - толщина покрытия, м;
Sгод – годовая производственная программа, м2/год;
r - плотность металла покрытия, кг/м3;
к1 – коэффициент учитывающий сложность геометрической формы детали (к1=1,3);
к2 – коэффициент учитывающий непроизводительные потери (к2=1,15).
mагод = 52500 × 7,5×10-6 × 7200 × 1,3 × 1,15 = 4238,3 кг.
4.6 Расчёт вытяжной вентиляции
Количество воздуха, отсасываемого от одной ванны, рассчитывается по формуле:
V = V0 × ктемп × ктокс × к1 × к2 × к3 × к4, (4.48)
где V0 – объём, зависящий от габаритов ванны, м3/ч;
ктемп – температурный коэффициент;
ктокс – коэффициент токсичности [13];
к1 – коэффициент, учитывающий вид бортового отсоса;
к2 – коэффициент, учитывающий наличие воздушного перемешивания;
к3 – коэффициент, учитывающий наличие полых шариков на поверхности раствора;
к4 – коэффициент, учитывающий наличие пены на поверхности раствора.
V0 = 1400 ×(0,53 × w × l / (w + l) + h)0,33 × w × l, (4.49)
где w – ширина ванны в случае отсосов с вертикальной щелью всасывания, м;
l – длинна ванны, м;
h – расстояние от зеркала электролита до середины щели всасывания бортового отсоса, м.
Для химических ванн:
V0 =1400×(0,53×0,63×1,25/(0,63+1,25)+0,2)0,33×0,63×1,25= 829,3 м3/ч.
Для электрохимических ванн:
V0 =1400×(0,53×0,8×1,25/(0,8+1,25)+0,2)0,33×0,8×1,25= 1082,4 м3/ч.
Температурный коэффициент рассчитывается по формуле:
ктемп = 1 + 0,0157 × (tр – tв), (4.50)
где tр – температура раствора, °С;
tв – температура воздуха, °С.
Пример расчёта для ванны обезжиривания:
V0 = 829,3 м3/ч; ктокс =1; к1 =1; к2 =1; к3 =1; к4 =0,5.
ктемп = 1 + 0,0157 × (60 – 20) = 1,628
V = 829,3 × 1,628 × 1 × 1 × 1 × 1 × 0,5 = 675 м3/ч.
Результаты расчёта приведены в таблице 4.6.
Таблица 4.6 – Количество отсасываемого от ванн воздуха
|
Ванна |
V0, м3/ч |
Dt |
ктемп |
ктокс |
к1 |
к2 |
к3 |
к4 |
V, м3/ч |
|
Обезжиривание |
829,3 |
40 |
1,628 |
1 |
1 |
1 |
1 |
0,5 |
675 |
|
Тёплая промывка после обезжиривания |
829,3 |
30 |
1,471 |
0,5 |
1 |
1 |
1 |
1 |
610 |
|
Электрохимическое обезжиривание |
1082,4 |
40 |
1,628 |
1,6 |
1 |
1 |
1 |
0,5 |
1764,2 |
|
Тёплая промывка после электрохимического обезжиривания |
829,3 |
30 |
1,471 |
0,5 |
1,8 |
1 |
1 |
1 |
1098 |
|
Тёплая промывкапосле пассивации |
829,3 |
30 |
1,471 |
0,5 |
1,8 |
1 |
1 |
1 |
1098 |
|
Сумма: |
5245,2 |
5 Охрана труда и техника безопасности
ТЕХНИКА БЕЗОПАСНОСТИ ПРИ ХРАНЕНИИ И ТРАНСПОРТИРОВКЕ КИСЛОТ И ЩЕЛОЧЕЙ. Хранение кислот в цехе допускается только в специально отведенном помещении с кислотоупорными полом и стенами. Кладовая должна быть обеспечена надежным вентиляционным отсосом воздуха. Хранение кислот в открытых сосудах не допускается.
Каждую бутыль следует снабдить ярлыком с указанием наименования сорта, веса и ГОСТ; бутыли с кислотой требуется заполнять не более 9/10 их емкости.
Запас кислот в цеховых кладовых не должен превышать потребности 1—3 суток.
Опорожненные бутыли из-под кислоты перед возвращением на склад требуется промывать содовым раствором и ополаскивать водой. В опорожненных бутылях не должно оставаться на дне значительного количества кислоты. Опорожненные бутыли необходимо переносить всегда горлышком кверху во избежание ожога рук и ног при попадании капель оставшейся кислоты.
Погрузку, транспортировку и разгрузку кислот и щелочей необходимо осуществлять в спецодежде, состоящей из резиновых сапог, перчаток и фартуков.
ПЕРВАЯ ПОМОЩЬ ПРИ ОТРАВЛЕНИИ И ОЖОГАХ. Признаки отравления кислотами (азотной, серной и соляной): жгучая боль (жжение) во рту, пищеводе и желудке, бурые пятна в углах рта, рвота.
Необходимо: вызвать и поддерживать рвоту, пить молоко и слабые щелочи, жженую магнезию в смеси с водой и молоком, известковую, белковую и мыльную воду (за исключением соды), обильное питье.
Признаки отравления окислами: кашель, удушье, возбужденное состояние, сухость и острые боли гортани, обморочное состояние, рвота, жажда, боли в животе, бурная сердечная деятельность, изменение окраски кожного покрова. Действие отравления может проявиться через несколько часов.
Необходимо вынести пострадавшего в хорошо проветриваемое теплое помещение, освободить от стесняющей одежды, уложить на спину, обложить грелками, дать слабые щелочи — жженую магнезию в смеси с водой и молоком, известковой, белковой или мыльной водой, масло, обильное питье, лед.
При отравлении парами щелочей и их растворами — глотать кусочки льда, пить слабый раствор уксуса;
В случае ожога: щелочами — промыть пораженное место слабым раствором уксусной кислоты, водой и перевязать; кислотами — промыть пораженное место раствором соды, холодной водой, смазать вазелином и перевязать; концентрированной серной кислотой — обтереть пораженное место сухой тряпкой, промыть большим количеством воды, смазать вазелином и перевязать.
ПЕРВАЯ ПОМОЩЬ ПРИ ПОРАЖЕНИИ ЭЛЕКТРИЧЕСКИМ ТОКОМ. В гальванических цехах применяются силовые установки постоянного (3—12 в, а иногда и 60 в) и переменного (110 и 22/380 в) токов. Учитывая, что рабочие этих цехов по роду своей работы находятся в контакте с электролитами, следует уделить особое внимание вопросам техники безопасности при эксплуатации электрооборудования.
Электротехническое оборудование, а также предметы, на которых могут появляться при авариях или при движении и трении статические электрические заряды, должны быть надежно заземлены. У указанного оборудования должны быть ограждены движущиеся и вращающиеся детали (шкивы, валы, муфты, штоки). Обслуживающий персонал должен быть снабжен спецодеждой и, в частности, резиновыми сапогами и резиновыми перчатками. Все электротехнические установки, приборы и агрегаты, представляющие опасность для обслуживающего персонала, должны иметь надписи, помогающие избегать несчастных случаев. Помимо таких плакатов, как, например, «Не выключать — работают люди», «Под напряжением», «Высокое напряжение. Опасно для жизни», «Не трогать» и др., в цехах электрохимических покрытий должны вывешиваться инструкции по технике безопасности при обращении с источниками постоянного или переменного токов. Инструкция должна быть доведена до каждого работающего во время беседы или инструктажа.
Однако, поскольку даже при соблюдении этих мер в цехах электрохимических покрытий все же возможны несчастные случаи в результате поражения электрическим током, персонал цеха должен уметь оказывать в таких случаях первую помощь пострадавшему до прихода врача-специалиста.
Эта помощь должна выражаться в немедленном устранении очага поражения. При оказании первой помощи необходимо немедленно выключить ток на той части установки, к которой прикасается пострадавший, а если этого быстро сделать нельзя, то оторвать его от токоведущих частей установки или проводов, предварительно защитив себя подручными средствами от поражения. Для этого следует надеть галоши или резиновые перчатки, встать на сухую деревянную доску, обернуть руки сухой одеждой и т. п.
ПОЖАРНАЯ БЕЗОПАСНОСТЬ В ЦЕХАХ ЭЛЕКТРОХИМИЧЕСКИХ ПОКРЫТИЙ. Причиной пожаров могут быть неисправность электрических сетей, оборудования и предохранителей.
Для предотвращения аварий, вызванных токами короткого замыкания, на распределительных щитах устанавливают автоматы, которые мгновенно отключают участки сети, на которых произошло короткое замыкание.
Частыми причинами пожаров в гальванических цехах являются также самовоспламенение органических веществ, обтирочных промасленных концов и тряпок, промасленная одежда и т. п. Воспламенение этих предметов может произойти также под действием сконцентрированных солнечных лучей.
Пожары, возникающие по этим и другим причинам, могут быть быстро ликвидированы водой, воздушно-механической и химической пеной. Пена применяется для тушения легковоспламеняющихся жидкостей. Она представляет собой смесь газа и жидкости и имеет небольшую плотность 0,1—0,2 г/м3. Пена растекается по поверхности горящей жидкости, изолирует ее от пламени.
6 БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
22.
23.


