Лекарственные препараты
| Загрузить архив: | |
| Файл: ref-10733.zip (62kb [zip], Скачиваний: 162) скачать |
Содержание
Вопрос №2. Антибиотики. Тетрациклины. Структура. Отдельные представители. PAGEREF _Toc3582793 h 4
Антибиотики. PAGEREF _Toc3582794 h 4
Тетрациклины. Структура. PAGEREF _Toc3582795 h 6
Отдельные представители: PAGEREF _Toc3582796 h 7
Вопрос №1. Сульфаниламидные препараты. Какие препараты получены в результате модификации амидной группы белого стрептоцида?
Важным этапом в развитии химиотерапии до наступления эры антибиотиков надо считать создание мощных антимикробных средств, эффективных против граммположительных и граммотицательных бактерий, что связано с появлением сульфаниламидных препаратов.
Простейший представитель этой группы – амид сульфаниловой кислоты, или сульфаниламид (белый стрептоцид), был известен еще с 1908 г. как один из компонентов при синтезе красителей; его второе рождение произошло в 1935 г., когда Г. Домарк в германии открыл антимикробную активность пронтозила, или красного стрептоцида. Былоустановлено, что пронтозил неактивен in vitro, но проявляет эффектin vivo, поскольку при разложении в организме превращается в активный сульфаниламид. Механизм бактериостатического действия сульфамидов связан с их вмешательством в биосинтез фолиевой кислоты – соединения, которое необходимо для жизнедеятельности бактерий. Фолиевая кислота представляет собой N-птериол-L-глутаминовую кислоту; благодаря химическому сходству с парааминобензойной кислотой (ПАБК) сульфаниламиды блокируют ее включение в фолиевую кислоту. Нарушение же синтеза фолиевой кислоты препятствует образованию из нее фолиновой (5,6,7,8-тетрагидрофолиевой) кислоты, необходимой для синтеза пуриновых и пиримидиновых оснований нуклеиновых кислот. В тканях человека это не происходит, так как они утилизируют уже готовую фолиевую кислоту, чем и объясняется избирательность действия сульфаниламидов.
Ряд сульфаниламидных препаратов получен путем введения в сульфонамидную группу остатков гетероциклических оснований. Введение дополнительных заместителей позволяет пролоногировать действие препаратов, улучшить проникновение их в жидкости и ткани организма и тем самым увеличить эффективность действия.
Введение гетероциклицеских заместителей обычно осуществляют по реакции сульфонилхлорида с аминопроизводными гетероциклов:

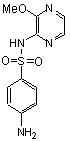
Сульфаниламидные препараты, полученные в результате модификации амидной группы белого стрептоцида:
Таблица 1
|
|
|
|
|
|
|
|
Бел. стрептоцид |
Сульгин |
Сульфадимезин |
Альбуцид |
Нурсульфазол |
Этазол |
|
|
|
|
|
|
|
|
Кр. стрептоцид |
Сульфа |
Сульфазин |
Уросульфан |
Сульфален |
Вопрос №2. Антибиотики. Тетрациклины. Структура. Отдельные представители.
Антибиотики
Антибиотики – это химические вещества, образуемые микроорганизмами, которые обладают способностью подавлять рост или даже разрушать бактерии и другие микроорганизмы. Это определение дано С. Ваксманом.
Однако З. В. Ермольева дает более широкое толкование этому понятию: “Антибиотики – вещества природного происхождения, обладающие выраженной биологической активностью. Они могут быть получены из микробов, растительных и животных тканей, синтетическим путем”.
Микробиологические основы химиотерапии инфекционных заболеваний.
Каждый антибиотик обладает специфическим избирательным действием на определенные виды микробов. Благодаря такому избирательному действию многие антибиотики способны подавлять жизнедеятельность патогенных микроорганизмов в безвредных для организма концентрациях. Такие антибиотики широко используют для лечения различных инфекционных болезней.
Основными продуцентами антибиотиков служат микроорганизмы, обитающие в почве и воде, где они постоянно вступают между собой в самые разнообразные взаимоотношения. Последние могут быть нейтральными, взаимовыгодными (например, деятельность гнилостных бактерий создает условия для деятельности нитрифицирующих бактерий), но очень часто они являются антагонистическими. И это понятно. Только таким путем в природе могло сложиться сбалансированное сосуществование громадного числа видов живых существ. И. И. Мечников предложил использовать антагонизм между бактериями на пользу человеку. Он, в частности, рекомендовал подавлять активность гнилостных бактерий в кишечнике человека, продукты жизнедеятельности которых, по его мнению, сокращают жизнь человека, молочнокислыми бактериями.
Механизмы микробного антагонизма различны. Они могут быть связаны с конкуренцией за кислород и питательные вещества, с изменением рН среды в сторону, неблагоприятную для конкурента, и т.д.
Одним из универсальных механизмов микробного антагонизма является синтез химических веществ-антибиотиков, которые либо подавляют рост и размножение других видов микроорганизмов (бактериостатическое действие), либо убивают их (бактерицидное действие).
Требования, предъявляемые к антибиотикам.
Чтобы быть хорошим лечебным средством, антибиотик должен иметь, по крайней мере, некоторые обязательные свойства.
1.
2.
3.
4.
5.
6.
Хотя, здесь есть и исключения. Речь идет о поиске таких антибиотиков, которые бы подавляли трансплантационный иммунитет. К числу последних относится циклоспорин А, который обладает мощным иммуносупрессивным действием. Однако его широкому применению препятствует цитотоксическое действие на почки.
Основные группы антибиотиков.
Антибиотики имеют различное химическое строение. Нашедшие применение в медицине антибиотики относятся к нескольким группам:
1. b-лактамные антибиотики;
2.
3.
4.
5.
6.
7.
8.
Тетрациклины. Структура
1.
2.

3.
4.
5.
6.
Отдельные представители:
Таблица 2
|
Название |
X |
R1 |
R2 |
R3 |
R4 |
|
Природные тетрациклины |
|||||
|
Тетрациклин |
H |
CH3 |
OH |
H |
NH2 |
|
Хлортетрациклин |
Cl |
CH3 |
OH |
H |
NH2 |
|
Окситетрациклин |
H |
CH3 |
OH |
OH |
NH2 |
|
7-Бромтетрациклин |
Br |
CH3 |
OH |
H |
NH2 |
|
6-Диметилтетрациклин |
H |
H |
OH |
H |
NH2 |
|
7-Хлор-6-диметилтетрациклин |
Cl |
H |
OH |
H |
NH2 |
|
2-Декарбоксамидо-2-ацетилтетрациклин |
H |
CH3 |
OH |
H |
CH3 |
|
7-Хлор-2-Декарбоксамидо-2-ацетилтетрациклин |
Cl |
CH3 |
OH |
H |
CH3 |
|
5-Окси-2-Декарбоксамидо-2-ацетилтетрациклин |
H |
CH3 |
OH |
OH |
CH3 |
|
Полусинтетические тетрациклины |
|||||
|
Ролитетрациклин |
H |
CH3 |
OH |
H |
|
|
Метациклин |
H |
CH2 |
H |
NH2 |
|
|
Миноциклин |
N(CH3)2 |
H |
H |
H |
NH2 |
Терапевтическое действие некоторых тетрациклиновых антибиотиков
Тетрациклин:
·
Тетрациклина гидрохлорид:
·
Окситетрациклина дигидрат:
·
Окситетрациклина гидрохлорид:
·
Метациклина гидрохлорид (полусинтетическое производное тетрациклина):
·
Доксициклина гидрохлорид (полусинтетическое производное окситетрациклина):
·
·
Вопрос №3. Противоопухолевые препараты. Механизм действия алкилирующих препаратов.
Известно несколько групп соединений, которые проявляют противоопухолевое действие, но при этом, как правило, затрагивают и нормальные клетки. Это антиметаболиты, цитостатические препараты (алкилирующие агенты, комплексы металлов, природные соединения – алкалоиды, антибиотики, ферменты, гормоны).
Антиметоболиты достаточно разнообразны по структуре; обычно они являются производными витаминов, гетероциклических оснований кислот, нуклеозидов. К антиметоболитам относят:
|
|
|
|
|
|
Метотрексат |
6-меркаптопурин |
Фторурацил |
|
|
|
|
|
|
|
Фторафур |
Цитарабин |
Тиазофурин |
Фопурин |
Наиболее многочисленной является группа цитостатических препаратов, включающая алкилирующие агенты (эмбихин, допан, сарколизин, циклофосфан, проспидин, спиробромин и др.), соединения, содержащие остаток этиленимина, нитрозометилмочевину и комплексы металлов.
Таблица 3
|
|
|
|
|
||
|
Эмбихин |
Сарколизин |
Допан |
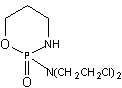
Циклофосфан |
||
|
|
|||||
|
Проспидин |
|||||
|
|
|||||
|
Спиробромин |
|||||
|
|
|
|
|||
|
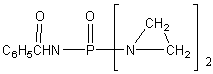
Тиофосфамид |
Имифос |
Бензотеф |
|||
|
|
|
||||
|
Цисплатин |
Нитрозометилмочевина |
||||
Одними из первых в качестве противоопухолевых средств стали применять производные бис-(b-хлорэтил)-амина. Поводом к использованию этих соединений послужили данные о способности азотистого иприта, или трихлорэтиламина, вызывать выраженную лейкопению и аплазию костного мозга. В медицинской практике используются менее токсичные производные бис-(b -хлорэтил)-амина (циклофосфан, эмбихин и др.). Вслед за бис-(b -хлорэтил)-аминами были получены цитостатические алкилирующие соединения других химических групп: этиленимины, алкилированные cульфонаты, триазены, препараты платины, нитрозомочевины и др.
Алкилирующие агенты способны реагировать с нуклеофильными центрами белковых молекул, нарушая главным образом синтез ДНК, в меньшей степени синтез РНК. В результате нарушается жизнедеятельность клеток, блокируется их митоз. Высокой чувствительностью к этим веществам обладают ядра клеток гиперплазированных (опухолевых) тканей и лимфоидной ткани. В то же время производные бис-(b-хлорэтил)аминов легко взаимодействует с нуклеопротеидами клеточных ядер кроветворных тканей, угнетая процесс кроветворения.
Хлорэтиламины обладают высокой токсичностью и в дозах, близких к лечебным, могут вызывать побочные явления, проявляющиеся в сильном угнетении костно-мозгового кроветворения и нарушениях функции желудочно-кишечного тракта. Такие препараты, как эмбихин, допан и другие применяют при лимфогрануломатозе, миелолейкозе, хроническом лимфолейкозе.
Сарколизин обладает алкилирующими свойствами и подавляет развитие гиперплазированных тканей. Применяют для лечения семиномы яичка, ретикулосаркомы, миеломной болезни и др.
Проспидин и спиробромин применяют при лечении рака гортани. Они не проявляют явного угнетающего действия на кроветворение, однако обладают иммунодепрессивными свойствами.
Этиленимины по механизму действия близки к производным бис-(b-хлорэтил)-амина. Они блокируют митотическое деление клеток с помощью образования поперечных связей между цепями молекулы ДНК, что препятствует ее репликации.
Механизм противоопухолевого действия производных платины (карбоплатина, цисплатина) связан со способностью к бифункциональному алкилированию нитей ДНК, ведущему к длительному подавлению биосинтеза нуклеиновых кислот и гибели клеток.
Список используемой литературы
1. Евстигнеева Р.П. Тонкий органический синтез. М.: Химия, 1991. 184 с.
2. Овчинников Ю.А. Биоорганическая химия. М.: Просвещение, 1987. 815 с.
3.
4.